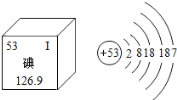
��Ŀ����
����Ŀ����ѧ��ȤС�����÷��ռ������Na2CO3��NaCl��MgCl2��CaCl2�ȣ���Na2CO3��10H2O��
����ȡ���̡�
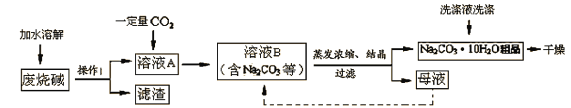
��������ϡ���Na2CO3+H2O+CO2��2NaHCO3
��2NaHCO3![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
����NaHCO3��Һ�м���BaCl2��Һ���ɷ�����Ӧ��2NaHCO3+BaCl2��BaCO3��+2NaCl+ H2O+CO2��
��̼���Ƶı�����Һ�ڲ�ͬ�¶��������ľ�������ͼ��ʾ��
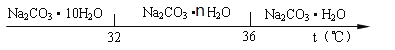
���������ۡ�
��1��������Ҫ�ɷ�ΪMg��OH��2�� ������Mg��OH��2�Ļ�ѧ����ʽ ��
��2����������ʹ�õIJ��������У��ձ��� �Ͳ�������
��3��ȡ������ҺB������BaCl2��Һ����ֻ�ϣ����۲쵽 ������������ҺB�к�NaHCO3��
��4���ᾧ����ʱ���¶������ �档
��5����ĸҺ������������������·��ѭ��ʹ�ã�ԭ���� ��ѡ����ţ���
�١�ĸҺ������Na2CO3
�ڡ�ĸҺ�����ѭ����NaCl��������
�����ȷ����
��6��ȡ�����ֲ�Ʒ����ˮ�ܽ⣬������ ��ѡ��������ţ���ͬ������ֽ��裬�ټ����� ��������֤�����в���NaCl��
��AgNO3��Һ ��ϡ���� ��ϡ����
��7����ȤС��ͬѧȡ32.8g����ֲ�Ʒ������ͼ��ʾװ�ã��г�����ʡ�ԣ�����ʵ�飺
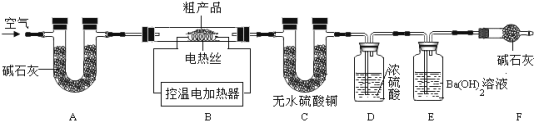
��������1��Na2CO3��10H2O������32������ʼ�ֽ�ʧˮ����ּ��ȿ���ȫʧˮ��NaHCO350��ʱ��ʼ�ֽ�270��ʱ��ȫ�ֽ⣻Na2CO3���Ȳ��ֽ⡣
��������2��Ba(OH)2��Һ������CO2��Ba(OH)2+CO2=BaCO3��+H2O
��ʵ��ǰҪ�� ����װ��ֲ�Ʒ��
װ��A�������� ��
���ֲ�Ʒ������270������ ����װ�ñ�ż�������֪�ֲ�Ʒ�к�NaHCO3�����C��D������m1��E��������m2����m1��m2 �����������=��������9��22��
ʵ����m2��1.1g���������32.8g�ֲ�Ʒ�к���NaHCO3������Ϊ g��
����������36��ʱ�����B��ʣ�����27.4g�����ʣ������� ���ѧʽ����NaHCO3�Ļ������˿�2�֣�
���𰸡���1��CaCO3�� 2Na OH+ MgCl2=2NaCl+Mg��OH��2��
��2��©��
��3����������
��4��32
��5����
��6���ۡ���
��7�������װ�õ������� ���տ����еĶ�����̼��ˮ����
��C�б�Ϊ��ɫ��E�в�����ɫ���� �� 4.2 ��Na 2CO3��7H2O
��������
������������������ۡ���1���ռ������������Ȼ�þ��Ӧ������������þ������̼�������Ȼ��Ʒ�Ӧ������̼��Ƴ�������������Ҫ�ɷ�Ϊ������þ��̼�������2������������Ҫ��������Һ����룬��Ϊ���˲���������Ҫ©������3���Ȼ�����̼�����Ʒ�����Ӧ���£�2NaHCO3+BaCl2��BaCO3��+2NaCl+ H2O+CO2�������������ݺͰ�ɫ����ʱ��֤����ҺB�к�̼�����ƣ���4���ᾧ����ʱ���¶������32��
��5����ĸҺ������������������·��ѭ��ʹ�ã�ԭ���ǡ�ĸҺ�����ѭ����NaCl������������ѡ��;�����ȷ�����ȼ����ᣬ��ȥ̼���ƣ�Ȼ�������������Һ�������Ȼ��ƣ����������Ȼ��Ʋ�����ɫ�������Ұ�ɫ�����Ȼ���������ϡ���ᡣ��ʵ��ǰҪ�ȼ��װ�õ������ԣ��ټ���ֲ�Ʒ����ʯ�������տ����е�ˮ�ֺͶ�����̼��������������ֲ�Ʒ������270��ʱ����ȫ�ֽ⣬����ˮ��������̼��̼���ƣ�������̼��ʹ����ʯ��ˮ����ǣ���ˮ����ͭ��ˮ��Ϊ��ɫ��̼���������ȷֽ����ˮ��̼���ƾ���ֽ�Ҳ�����ˮ��C��D������m1��������ˮ��������E��������m2��̼���������ȷֽ����������̼������2NaHCO3 ![]() Na2CO3+H2O+CO2�����м��㣬ˮ�Ͷ�����̼������Ϊ9��:22������m1��m2��9��22��
Na2CO3+H2O+CO2�����м��㣬ˮ�Ͷ�����̼������Ϊ9��:22������m1��m2��9��22��
�⣺��̼����������ΪX
2NaHCO3 ![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
168 44
X 1.1g
168/44=X/1.1g X=4.2g
����������36��ʱ,̼���������Ȳ���ֽ⣬��������̼����������Ϊ4.2g��֪���ֲ�Ʒ�к���̼�����ƾ���28.6g����̼��������=28.6g����106/136��100%��=10.6g����������36��ʱ�����B��ʣ�����27.4g��̼�����Ƶ�����Ϊ4.2g����̼���ƾ�������=27.4g-4.2g=23.2g ������ʽΪ��
23.2g ����106/106+18n��100%��=10.6g n=7����ѧʽΪ��Na 2CO3��7H2O