题目内容
【题目】用图所示装置研究二氧化碳的性质。其中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。
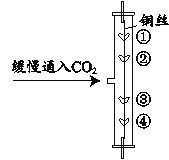
(1)说明CO2密度大于空气的实验现象为_____;除此之外,该实验还能研究的二氧化碳的性质是_____。
(2)某同学将变红了的棉球用吹风机烘干后,观察到棉球又变回紫色。但是,他认为此现象不足以说明“碳酸受热发生化学反应”,理由是_____。
【答案】④处湿润的紫色棉球先变红,①处后变红 二氧化碳与水反应生成酸性物质 碳酸受热挥发也可以使棉球又变回紫色(或其他合理答案)
【解析】
(1)二氧化碳的密度比空气的密度大,故会先充满玻璃管的下部,故④处的湿润棉球先变红,①处后变红。湿润棉球变红,而干燥棉球不变红,说明二氧化碳能与水反应生成碳酸。
(2)碳酸受热挥发也可以使棉球又变回紫色,故不能说明碳酸受热分解生成二氧化碳和水。

 阅读快车系列答案
阅读快车系列答案【题目】据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。

(提出问题)从废旧手机中可以回收到哪些有价值的金属?如何回收?
(查阅资料)
i.手机电路板中的金属及其价格如下表所示:
种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
市场价格($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”。
ii.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后;NiCl2溶液为绿色。
Iii.2Cu+O2+2H2![]() 2CuSO4+2H2O
2CuSO4+2H2O
(实验方案)
第一步:选择值得回收的金属。
依据资料i中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,原因是:①它们的市场价格较高;②_____。
第二步:设计实验分离、回收部分金属。
序号 | 实验步骤 | 实验现象 |
I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
II | 将金属电路放入烧杯中,加入足量稀盐酸浸泡 | _____ |
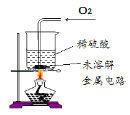
III | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如图所示装置中,进行实验。
| 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
IV | 过滤III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
V | _____ | 得到红色固体 |
(问题讨论)
(1)由步骤I中的现象,可推知的焊锡的物理性质是_____。
(2)步骤II对应的实验现象是_____。
(3)步骤II所得溶液中,一定含有的金属元素是_____。
(4)步骤V的操作是_____。
(反思交流)
为了确认步骤IV中滤纸上的金属成分,应进一步查阅的资料为_____。
【题目】实验小组研究制备Cu(OH)2的条件并探究其稳定性。
(查阅资料)两种含铜化合物的部分性质如下表所示。
化合物 | Cu(OH)2 | Cu4(OH)6SO4 | CuO |
颜色 | 蓝色 | 绿色 | 黑色 |
在水中的溶解性 | 难溶 | 难溶 | 难溶 |
(进行实验)
实验1:室温下,取16%CuSO4溶液和4%NaOH溶液进行实验。
| 序号 | CuSO4溶液体积/mL | NaOH溶液体积/mL | 实验现象 |
1-1 | 2 | 2 | 产生浅绿色沉淀 | |
1-2 | 2 | 4 | 产生蓝色沉淀 混有少量浅绿色沉淀 | |
1-3 | 2 | 6 | 产生蓝色沉淀 |
实验2:将1-3所得混合物过滤,得到蓝色沉淀,将沉淀洗涤、干燥后置于恒温烘箱中,3h后观察并记录实验现象。
序号 | 2-1 | 2-2 | 2-3 | 2-4 | 2-5 |
烘箱温度/oC | 40 | 50 | 60 | 70 | 80 |
固体是否变黑 | 不变黑 | 不变黑 | 不变黑 | 变黑 | 变黑 |
实验3: 重复实验1-3,将所得混合物置于不同水浴温度下,记录实验现象。
序号 | 3-1 | 3-2 | 3-3 | 3-4 |
水浴温度/oC | 0 | 30 | 60 | 90 |
出现黑色沉淀的时间 | 1h | 3min | 25s | 2s |
(解释与结论)
(1)CuSO4溶液与NaOH溶液反应制Cu(OH)2的化学方程式为_____。
(2)实验1-1反应得到浅绿色沉淀的主要成分是______。
(3)由实验1
(4)实验2固体变黑的原因是_____(用化学方程式解释)。
(5)实验3的结论是_____。
(反思与评价)
(6)对比实验2和实验3,得出的结论是_____。