题目内容
【题目】相同质量的下列物质①Zn②ZnO③Zn(OH)2④ZnCO3,分别跟质量分数都相同且适量的稀盐酸充分反应,所得溶液的溶质质量分数的关系正确的是( )
A.①>②>③>④B.④>③>②>①C.①>②=④>③D.④>①>②=③
【答案】C
【解析】
设:①Zn②ZnO③Zn(OH)2④ZnCO3的质量都是m,稀盐酸的溶质的质量分数为n,
①设参加反应的氯化氢的质量为x1,生成氯化锌的质量为y1,生成氢气的质量为a1,
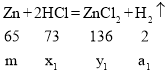
![]()
x1=![]() y1=
y1=![]() a1=
a1=![]()
所得溶质的质量分数为:
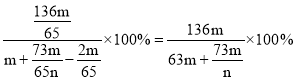
②设参加反应的氯化氢的质量为x2,生成氯化锌的质量为y2,
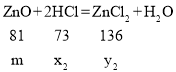
![]()
x2=![]() y2=
y2=![]()
所得溶质的质量分数为:
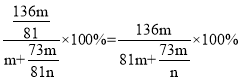
③设参加反应的氯化氢的质量为x3,生成氯化锌的质量为y3,生成水的质量为a3,
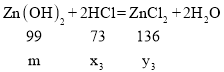
![]()
x3=![]() y3=
y3=![]()
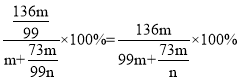
④设参加反应的氯化氢的质量为x4,生成氯化锌的质量为y4,生成水的质量为a4,生成二氧化碳的质量为b,
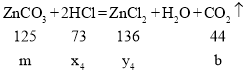
![]()
x4=![]() y4=
y4=![]() b=
b=![]()
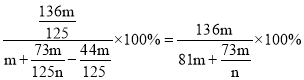
即:①>②=④>③
故选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目