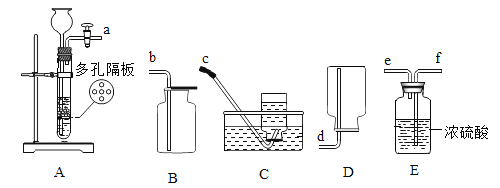
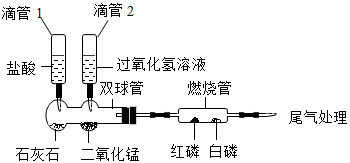
题目内容
【题目】有一包不纯的固体烧碱,其中可能含有Na2SO4、MgSO4、Ba(OH)2、NaCl中的一种或几种,取少量烧碱样品,按下图所示步进行实验:
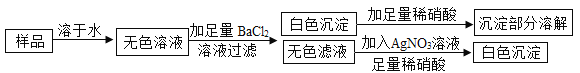
由此可推知该固体烧碱中一定含有_____;一定不含有_____。
【答案】Na2SO4 MgSO4、Ba(OH)2
【解析】
硫酸根离子和钡离子反应会生成不溶于酸的硫酸钡沉淀,氢氧根离子和镁离子反应会生成氢氧化镁沉淀,氢氧化钠变质生成的碳酸根离子和钡离子反应生成溶于酸的碳酸钡沉淀,氯离子和银离子反应生成不溶于酸的氯化银沉淀 ,样品溶于水,得到无色溶液,所以样品中一定不含硫酸镁;加入氯化钡生成白色沉淀,部分溶于硝酸,所以样品中一定含有硫酸钠,同时可判断样品中一定不含氢氧化钡;向无色溶液中加硝酸银溶液生成白色沉淀,说明溶液中有氯离子,但氯化钡引入了氯离子,所以不能确定样品中是否含有氯化钠,所以该固体烧碱中一定含有Na2SO4;一定不含有MgSO4、Ba(OH)2。

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目