题目内容
【题目】氧化锌软膏用于急性或亚急性皮炎、湿疹、痱子及轻度、小面积的皮肤溃疡,其有效成分氧化锌(ZnO)是一种白色固体。一种工业生产药用高纯氧化锌的流程如图:
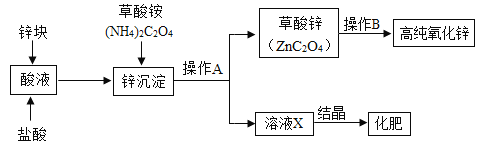
(1)“酸溶”所达到的目的是将锌块转化为可溶于水的______(填产物名称)。
(2)由草酸铵推测草酸的化学式为______。“锌沉淀”过程中发生反应的化学方程式为______。
(3)“操作A”的名称是______;溶液X结晶所得化肥是该工艺有价值的副产品,证明它是一种氮肥的方法是取少量样品与______混合、研磨,能嗅到氨味。
(4)“操作B”是高温灼烧,该过程除生成氧化锌外,还有两种气态碳氧化物生成,则草酸锌分解的化学方程式为_____。
【答案】氯化锌 C2H2O4 ZnCl2+(NH4)2C2O4=ZnC2O4↓+2NH4Cl 过滤 氢氧化钙 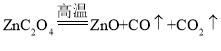
【解析】
(1)锌和盐酸反应生成氯化锌和氢气,所以“酸溶”所达到的目的是将锌块转化为可溶于水的氯化锌;
(2)化学反应前后,元素种类不变,由草酸铵推测草酸的化学式为C2H2O4,氯化锌和草酸铵反应生成草酸锌和氯化铵,化学方程式为:![]() ;
;
(3)过滤可以将不溶性固体从溶液中分离出来,所以“操作A”的名称是过滤,铵态氮肥和碱混合研磨会生成氨气,所以取少量样品与氢氧化钙混合、研磨,能嗅到氨味;
(4)草酸锌在高温的条件下生成氧化锌、一氧化碳和二氧化碳,化学方程式为: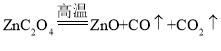 。
。

【题目】废铁屑主要成分是铁,还有少量铁锈(Fe2O3),硫酸亚铁的生产工艺如图所示。
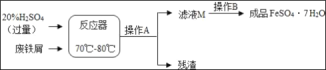
(1)在反应器中除发生Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,Fe2(SO4)3+Fe═3FeSO4这两个反应外,还会发生另外一个反应,化学方程式为:_____,反应器要加强通风,严禁烟火,其原因是:_____。
(2)将成品在有氧条件下焙烧,可转化为Fe2O3、SO2和SO3.为了提高SO3的产率,某实验小组进行了系列探究,实验数据如下:
编号 | 空气通入量/Ls﹣1 | 温度/℃ | SO2产率% | SO3产率/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
①本实验主要研究了哪些因素对SO3产率的影响_____。
②根据上表数据,生产过程中采用实验_____(填编号)的提取条件最合理。
③分析上表数据,空气的通入量对SO3的产率的影响规律是_____。