题目内容
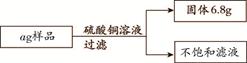
请根据下图所示实验过程和数据,计算反应后溶液中H2SO4的质量。


0.2 g
设生成氢气的质量为x,消耗H2SO4的质量为y, 加入稀硫酸的质量为z。
Zn + H2SO4=ZnSO4+H2↑
65 98 2
6.5 g y x
65∶2 ="6.5" g∶x,x="0.2" g
65∶98 ="6.5" g∶y,y="9.8" g
z+6.5 g="106.3" g+0.2 g,z="100" g
剩余H2SO4的质量="100" g×10% - 9.8 g ="0.2" g
Zn + H2SO4=ZnSO4+H2↑
65 98 2
6.5 g y x
65∶2 ="6.5" g∶x,x="0.2" g
65∶98 ="6.5" g∶y,y="9.8" g
z+6.5 g="106.3" g+0.2 g,z="100" g
剩余H2SO4的质量="100" g×10% - 9.8 g ="0.2" g

练习册系列答案
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目