题目内容
【题目】“物质的组成与结构决定物质的性质”是化学科学中的重要观点。按照这一观点讨论下面的问题。
【1】酸溶液具有一些共同的化学性质,是因为酸溶液中都含有的离子是 ;碱溶液也具有一些共同的化学性质,是因为碱溶液中都含有的离子是 。
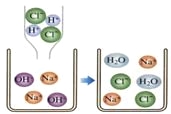
【2】写出下图所示的反应方程式 , 该反应前后,溶液中减少的离子是 。
【3】100g20%的氢氧化钠溶液中含有氢氧化钠的质量是 g,与足量的稀盐酸反应,生成氯化钠的质量是 g。
【答案】
【1】氢离子(1分) 氢氧根(1分)
【2】NaOH+ HCl =NaCl+ H2O (2分) H+(氢离子)、OH-(氢氧根)(1分)
【3】20g(2分) 29.3g(或29.25g)(2分)
【解析】
(1)酸溶液中都含有氢离子,碱溶液中都含有的离子是氢氧根,(2)酸碱反应的实质就是氢离子和氢氧根离子反应生成水分子,所以溶液中减少的离子是H+(氢离子)、OH-(氢氧根),(3)溶质质量=溶液质量*溶质质量分数=100g*20%=20g,设与足量的稀盐酸反应,生成氯化钠的质量是X克,
NaOH+ HCl =NaCl+ H2O,
40
【1】5
20g X
40/
【2】5=20g/x,解得X=
【3】25g

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目