题目内容
【题目】已知A-F是初中常见的化学物质,其中A为胃酸的主要成分,A、B、C、D都由两种元素组成,B、C、D、E、F含有同一种元素,它们在一定条件下的转化关系如图所示。“——”表示两种物质间能发生反应,“→”表示两种物质见能够转化,部分反应物或生成物以及反应条件已略去,请回答下列问题:
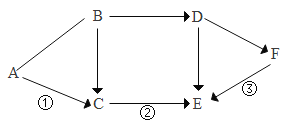
(1)C物质的化学式是_____;
(2)D转化为F的化学方程式:_____。
【答案】H2O CO2+2NaOH═Na2CO3+H2O
【解析】
A为胃酸的主要成分,所以A是盐酸;A、B、C、D都由两种元素组成,B、C、D、E、F含有同一种元素,B如果是氧化铁,氧化铁和稀盐酸反应生成水和氯化铁,稀盐酸和碱、金属氧化物反应有水生成,氧化铁和一氧化碳在高温条件下反应生成二氧化碳和铁,二氧化碳和氢氧化钙反应生成碳酸钙沉淀,二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故C是水,D是二氧化碳,E是碳酸钙,F是碳酸钠,经验证,推断正确。
(1)由分析可知,C是水,化学式为H2O;故填:H2O;
(2)D转化为F是二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O;故填:CO2+2NaOH═Na2CO3+H2O。

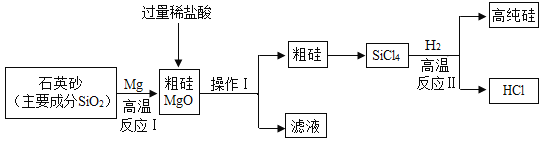
【题目】化学学习小组进行“铝和酸溶液反应的探究”的活动。用铝片分别和氢离子浓度相同的稀盐酸、稀硫酸反应,发现铝片和稀盐酸反应现象非常明显,而和稀硫酸却几乎不反应。
(提出问题)是什么原因导致两者的差异?
两种酸中氢离子浓度相同,那么存在的差异就可能跟H+所处的环境不同有关(如阴离子的不同)。
(作出猜想)猜想一:Cl-能促进金属铝与H+的反应。
猜想二:_____。
猜想三:铝表面的致密氧化膜有保护作用,使H+与铝不易接触。
为了验证上述假设,经充分讨论,大家设计了如下实验方案进行验证。
(查阅资料)已知 9.8%H2SO4 溶液和 7.3%HCl 溶液中 H+浓度相同。
(设计实验)
① | 9.8%H2SO4溶液5mL+铝片 | 不加其他试剂(对比) | 无气泡 |
② | 9.8%H2SO4溶液5mL+铝片 | 加入_____溶液 | 有较多气泡 |
③ | 9.8%H2SO4溶液5mL+铝片 | 加入 0.5mL Na2SO4 溶液 | 无气泡 |
④ | 7.3%HCl 溶液 5mL+铝片 | 加入_____溶液 | 有较多气泡 |
⑤ | 7.3%HCl 溶液 5mL+铝片 | 不加其他试剂(对比) | 有较多气泡 |
由实验②③得出猜想_____成立;由④⑤得出猜想_____不成立。为了验证猜想一成立,小明认为只需要在 5mL 9.8%H2SO4 溶液和铝片中加入_____,并与实验①对比即可。
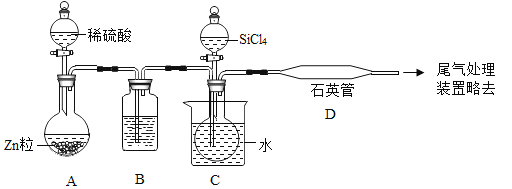
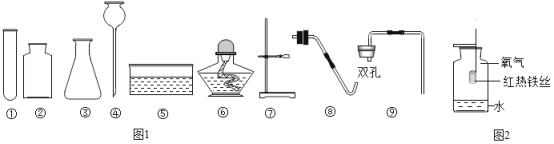
(实验拓展)对于有气体生成的化学反应,我们可以用产生气体的速率来比较反应速率。为准确比较,应该测量收集相同体积气体所需的_____,因此,上述收集氢气应该采用_____法。
为了真实地观察未打磨的铝片与稀盐酸反应的情况,小红用压强传感器测量集气瓶中气体压强的变化,如图所示。

请解释曲线变化的原因:
OA 段_____;AB 段_____;BC 段_____。指出反应结束并恢复到常温时集气瓶内的压强值约为_____kpa。