题目内容
【题目】宏观和微观相联系是化学独特的思维方式。
(1)物质性质反映其组成和结构。从宏观进入微观,探索物质变化规律。
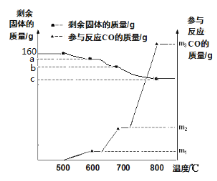
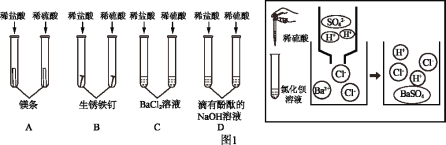
①不同酸具有相似的化学性质,但性质也存在差异。图1中不能体现酸的通性的是_____(填字母序号,下同);写出B中稀盐酸与铁锈反应的化学方程式_____;C中稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,据图从微粒的角度分析写出该反应的实质是_____。
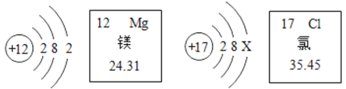
②一杯水中氢元素与氧元素的质量比和1个水分子中氢原子与氧原子的质量比_____(填“相等”或“不相等”)。
(2)物质组成和结构决定其性质。从微观进入宏观,探索物质变化规律。
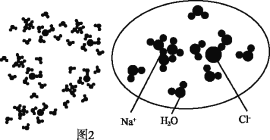
①图2圆圈中表示这杯氯化钠溶液的构成,则该氯化钠溶液中溶质和溶剂的质量比是_____。
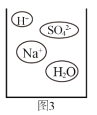
②通过分析组成和结构,可以预测物质的某些性质。根据图3硫酸氢钠溶液的微观图示,分析推测NaHSO4的性质,其中合理的是_____。
A 其水溶液能使紫色石蕊试液变红
B 其水溶液能与金属锌反应生成氢气
C 其水溶液能与硝酸钡溶液反应生成硫酸钡沉淀
D 其水溶液能与金属镁发生置换反应,得到金属钠
【答案】C Fe2O3+6HCl=2FeCl3+3H2O 溶液中的Ba2+和SO42-反应生成BaSO4沉淀 相等 13:40 ABC
【解析】
(1)①酸的通性是溶液中H+体现的,C中参与反应的是SO42-,所以没有体现酸的通性。硫酸和BaCl2溶液反应的微观本质从图中可以看出是溶液中的Ba2+和SO42-反应生成BaSO4沉淀。B中稀盐酸与铁锈反应生成氯化铁和水,其化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;C中稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,根据图从微粒的角度可知,其反应的实质是:溶液中的Ba2+和SO42-发生复分解反应生成BaSO4沉淀和HCl;故填:C;Fe2O3+6HCl=2FeCl3+3H2O;溶液中的Ba2+和SO42-反应生成BaSO4沉淀
②一杯水中由水组成,氢元素与氧元素的质量比为2:16和1个水分子中氢原子与氧原子的质量比为2:16;故填:相等
(2)①从图中可以看出,每个Na+和Cl-周围共有10个水分子,所以溶液中溶质和溶剂的质量比是58.5:(18×10)=13:40;故填:13:40
②NaHSO4溶液中含有Na+、H+、SO42-三种离子,因此NaHSO4溶液的性质由三种离子来体现,A、B选项是H+的性质,C选项是SO42-的性质;Mg不能置换出Na,说法错误。故填:ABC

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案