题目内容
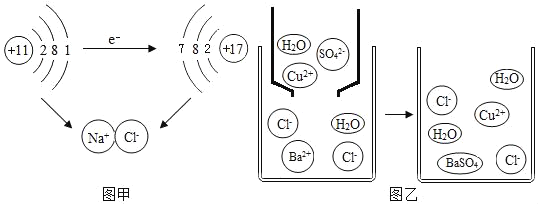
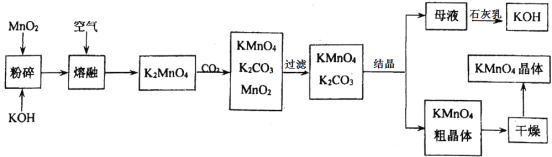
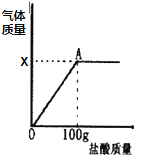
【题目】根据下图的有关信息,下列说法正确的是

A. 镁离子(Mg2+)的核内有12个质子B. 镁离子与氯离子的电子层数相同
C. 氯原子的核电荷数为35.45D. X=8时,该微粒带一个单位正电荷
【答案】A
【解析】
A、圆圈内的数字表示原子核内的质子数;
B、分析镁离子和氯离子的结构示意图并进行比较;
C、核电荷数=原子核内质子数=原子序数;
D、分析镁离子和氯离子所带电荷情况。
A、圆圈内的数字表示原子核内的质子数,原子变成离子,得失的是核外电子,质子数不变;故镁离子(Mg2+)核内有12个质子,选项A正确;
D、镁原子失去两个电子变成镁离子,电子层数为2;氯原子的最外层电子数>7,在化学反应中,易得1个电子变成氯离子,电子层数为3,所以二者电子层数不同,选项B不正确;
C、氯原子的核电荷数应等于原子序数,应为17,选项C不正确;
D、X=8时,氯原子得1个电子变成氯离子,该微粒带负电荷,选项D不正确。故选A。

【题目】白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究。
(查阅资料)白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3 ·yCaCO3。(杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一、定性探究:白云石粉的成分和性质
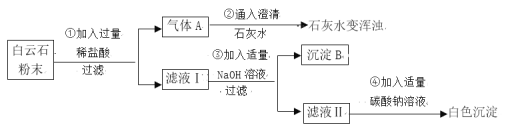
(实验分析)
(1)由步骤①②的现象可得出白云石粉中一定含有的离子是____________(填离子符号)。
(2)步骤③生成氢氧化镁的化学方程式是________________________________。该反应属于______(填写化学反应基本类型)。
(3)滤液Ⅱ中的溶质是_________________________。
(结 论)综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成。
(实验质疑)小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究。
二、定量探究:白云石的组成
(查阅资料)碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸镁与碳酸钙的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解。
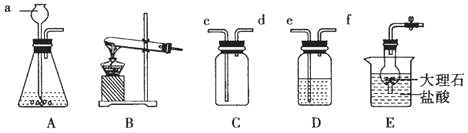
(实验设计)为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:
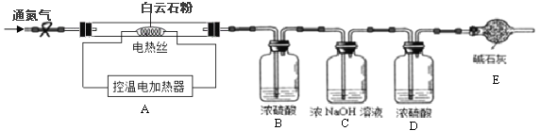
(实验步骤)①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量。
实验数据记录如下表:
B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | |
反应前 | 50.0 | 100.0 | 50.0 |
700℃ | 50.0 | 102.1 | 50.1 |
1000℃ | 50.0 | 106.3 | 50.3 |
(实验分析和数据处理)
(4)装置D的作用是______________;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是_______________。
(6)计算白云石中碳酸镁的质量分数。(写出计算过程):_______________。
(7)设计实验证明白云石粉已完全分解的实验方法是_____________________________(写出实验方法、现象)
(8)白云石(xMgCO3 ·yCaCO3)中的 x:y=___________(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值________(填偏大、偏小或不变)。