题目内容
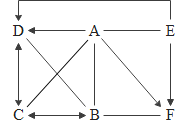
【题目】A、B、C、D、E、F六种物质为初中常见物质且均含有氧元素。A、B、E、F是不同种类别的物质,其中一种为配制波尔多液的原料,A、F含有两种相同元素且这两种元素质量比为1:2,其转化关系如图所示:
(1)请写出两种物质的化学式:D、________________;F、______________;
(2)过量的E和A反应的实验现象为_________________________。
(3)B→C的化学方程式为:____________________。
【答案】CO2 CuSO4 黑色固体部分溶解,溶液由无色变为蓝色 ![]()
【解析】
由题目信息可知,ABEF中存在硫酸铜或者氢氧化钙中的一种,而A、F含有两种相同的元素,且质量比为1:2,常见的主要为硫与氧元素,所以A、F中含有硫元素和氧元素,而硫酸铜正好满足此条件,所以A、F中存在硫酸铜,硫酸铜属于盐,其性质只能与碱反应,所以不能是A,因此F为硫酸铜,A中含有硫元素和氧元素,且可以与四种不同类型的物质反应 ,那A只能是酸,所以A为硫酸,A为酸,F为盐,所以B和E属于碱和氧化物,硫酸铜可以与碱反应,所以B为碱,常见为氢氧化钠,E为氧化物,且F含有铜元素,所以E为氧化铜,B氢氧化钠与C可以相互转化制备,推出C为碳酸钠,且碳酸钠与A硫酸也可以反应,而碳酸钠与D可以相互转化制备,符合要求的D为二氧化碳,同时E氧化铜与一氧化碳反应可以生成铜和二氧化碳,所以可以断定D为二氧化碳,所以A为硫酸,B为氢氧化钠,C为碳酸钠,D为二氧化碳,E为氧化铜,F为硫酸铜。
(1)根据分析可知D为二氧化碳,化学式为CO2;F为硫酸铜,化学式为CuSO4;
故答案为:CO2;CuSO4。
(2)E为氧化铜,A为硫酸,E过量,说明氧化铜可以部分溶解,生成硫酸铜,硫酸铜溶液为蓝色,但是不能全部溶解,所以可以看到黑色固体部分溶解,溶液变为蓝色;
故答案为:黑色固体部分溶解,溶液变为蓝色。
(3)有B氢氧化钠生成C碳酸钠,氢氧化钠与二氧化碳反应生成碳酸钠和水,据此书写化学方程式;
故答案为:![]() 。
。

【题目】氢化钙(CaH2)是一种白色细颗粒状固体,能与水发生剧烈反应,其反应的化学方程式为:![]() ,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是_____。为进一步确定滤液中所含溶质的成分,他们进行了以下实验探究。
,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是_____。为进一步确定滤液中所含溶质的成分,他们进行了以下实验探究。
[提出猜想]猜想一: NaOH
猜想二: NaOH 和Ca(OH)2
猜想三: NaOH、Na2CO3
猜想四: NaOH、 Na2CO3、 Ca(OH)2
经过讨论,大家一致认为猜想四不合理,理由是(用化学方程式表示)______。
[实验验证]
实验 | 现象 | 结论 |
(1)取少量滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想___不成立 |
(2)另取少量滤液,向其中加入______ | _____ | 猜想三成立 |
[反思与拓展]若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和___。