题目内容
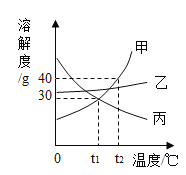
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A. 甲和丙的溶解度相等
B. 降温可使丙物质的不饱和溶液变成饱和溶液
C. t1℃时,甲、乙和丙各30g分别加入100g水中,均形成饱和溶液
D. t2℃时,将15g甲物质加入50g水中,再降温到t1℃时,所得溶液溶质的质量分数不变
【答案】D
【解析】
A、在比较物质的溶解度时,需要指明温度,故A错误;
B、丙物质的溶解度随温度的降低而增大,所以升温可使丙物质的不饱和溶液变成饱和溶液,故B错误;
C、t1℃时,乙物质的溶解度大于30g,甲、丙物质的溶解度等于30g,所以甲、乙和丙各30g分别加入100g水中,甲、丙形成饱和溶液,乙形成不饱和溶液,故C错误;
D、t2℃时,甲的溶解度为40g,将15g甲物质加入50g水中,形成的是不饱和溶液,再降温到t1℃时,甲物质的溶解度是30g,所以所得溶液溶质的质量分数不变,故D正确。
故选:D。

【题目】取一定量氯化镁溶液于烧杯中,将100g的氢氧化钠溶液平均分成五次加入烧杯中。在化学反应过程中对烧杯中的溶液和沉淀进行了多次过滤并称量。加入的氢氧化钠溶液和生成沉淀的质量关系记录如下表。
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入的氢氧化钠溶液质量/g | 20 | 20 | 20 | 20 | 20 |
沉淀总质量/g | 2.9 | 5.8 | 8.7 | 11.6 | 11.6 |
分析上表中的数据,完成下列问题:
(1)第_____次加完氢氧化钠溶液时,氯化镁和氢氧化钠恰好完全反应,此时生成沉淀质量为_____g。
(2)恰好完全反应时,称量所得氯化钠溶液质量为168.4g,则原氯化镁溶液中溶质的质量分数是____(请写出计算过程)。
【题目】化学源于生活,服务于生活。研究“水”可从多角度展开。
(1)水的电解
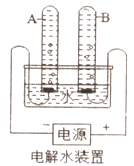
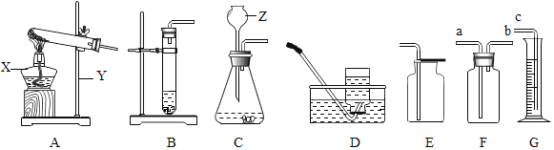
①宏观现象:按如图所示装置,通电一段时间后,试管A、B中产生气体的体积比约为_____,常在水中加入氢氧化钠的作用是_____。
②微观该反应中发生分解的微粒名称是_____,没有发生变化的粒子符号是_____。
(2)水的性质
将黄豆大小的金属钾放入盛有水的烧杯中,生成氢气和氢氧化钾。写出该反应的化学方程式_____。
(3)下列与水有关的实验中,实验和对应的解析都正确的是_____。
实验操作 | 解析 | |
A | 将燃烧的硫放盛有入留有少量水的氧气的集气瓶中 | 水可以吸收生成的二氧化硫,防止有毒气体外逸污染空气 |
B | 粗盐的提纯用到水溶解粗盐再过滤 | 根据物质在水中的溶解性的不同,把混合物进行分离除杂 |
C | 用水灭火 | 水能吸收热量,从而降低环境温度到可燃物着火点以下 |
D | 用氯化钠溶液进行导电性试验,观察小灯泡是否变亮 | 小灯泡变亮,说明氯化钠溶液中存在自由移动的离子 |