题目内容
【题目】碳酸钠广泛用于造纸、纺织、制革等工业,是一种重要的化工原料。我国侯德榜发明了将制碱与制氨结合起来的联合制碱法,为碳酸钠的工业化生产作出了巨大贡献。
(查阅资料)侯氏制碱法中主要反应:
Ⅰ.NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl
Ⅱ.2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
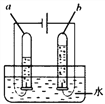
(实验探究)小明以粗盐配制饱和食盐水,并采用下列装置模拟制备碳酸氢钠,进而制得碳酸钠。
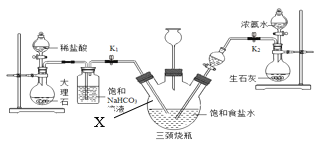
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。请回答下列问题:
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
(1)粗盐中除了含有泥沙等不溶性杂质,还含有少量的MgCl2等。若要除去粗盐中的MgCl2,可加入过量的NaOH溶液,写出对应的化学方程式_____,再过滤,然后向滤液中加入适量_____,得到氯化钠溶液。
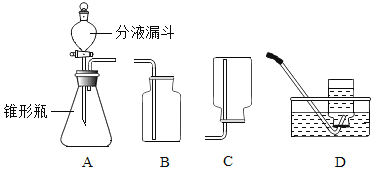
(2)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为_____。上述实验装置图中仪器X名称_____。
(3)三颈烧瓶上连接的长颈漏斗的主要作用是_____,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是_____;关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是_____。
(4)根据实验记录,计算t2时NaHCO3固体的分解率(已分解的NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程_____。
(拓展延伸)小华设计如图的实验装置测定某纯碱样品(含少量杂质NaCl)中碳酸钠的质量分数:取一定量的样品与足量稀硫酸反应,通过排饱和碳酸氢钠溶液测定生成CO2的体积,计算样品中碳酸钠的质量分数。

(已知常温常压下CO2的密度是1.977g/L)
(1)如果样品质量为5.3g,则实验中选用的量气管规格最合适的是_____(填字母)。
A 500mL B 1000mL C 1500mL D 2000mL
(2)若实验中测得碳酸钠质量分数偏小,下列可能的原因是_____。
a.装置漏气
b.读取数据时量气管的液面低于水准管的液面
c.反应结束后烧瓶中有CO2残留
d.读取数据时仰视读数
e.稀硫酸加入烧瓶占据体积
【答案】MgCl2+2NaOH=Mg(OH)2↓+2NaCl 稀盐酸 NaHCO3+HCl=NaCl+H2O+CO2↑ 三颈烧瓶 平衡气压 防止氨气逸出污染环境 使氨气充分反应 50% C ab
【解析】
[实验探究](1)氯化镁与过量氢氧化钠反应生成氯化钠和氢氧化镁沉淀,此时的溶液中除了氯化钠以外,还含有过量的氢氧化钠,可加入适量的盐酸将其中和为氯化钠;故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;稀盐酸;
(2)氯化氢气体溶于水形成盐酸,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳;上述实验装置图中仪器X名称是三颈烧瓶。故填:NaHCO3+HCl═NaCl+H2O+CO2↑;三颈烧瓶;
(3)长颈漏斗与外界空气相同,三颈烧瓶上连接的长颈漏斗的主要作用是平衡气压;有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,因为氨气与水反应形成氨水,氨水能与酸反应,故能防止防止氨气逸出污染环境;关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是形成酸性环境,利于使氨气充分反应。故填:平衡气压;防止氨气逸出污染环境;使氨气充分反应;
(4)设原混合物中碳酸氢钠的质量为x
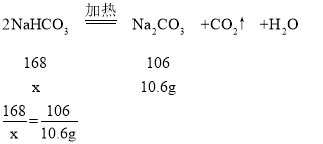
x=16.8g
完全反应时剩余固体减少16.8g-10.6g=6.2g。
t2时固体的质量减少了16.8g-13.7g=3.1g。
t2时固体的质量减少的质量为完全反应时的一半,则t2时NaHCO3固体的分解率为50%。
故填:50%;
[拓展延伸](1)如果5.3g样品全部为碳酸钠的质量,设生成二氧化碳的质量为y,则
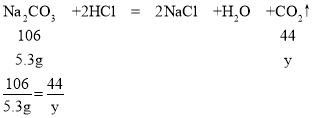
y=2.2g
根据V=![]() =
=![]() =1.1L=1100mL,则实验中选用的量气管规格最合适的是1500mL;故填:C;
=1.1L=1100mL,则实验中选用的量气管规格最合适的是1500mL;故填:C;
(2)a.装置漏气造成收集到的二氧化碳偏少,造成测定结果偏小;
b.读取数据时量气管的液面低于水准管的液面造成量气筒内的压强较大,造成收集的二氧化碳体积偏小,导致测定结果偏小;
c.进入量气筒中液体的体积等于锥形瓶中排出的气体体积,根据量气筒中液体的增加量,即为二氧化碳气体的体积,根据二氧化碳的体积算出碳酸钠的质量分数,因此烧瓶中若有CO2残留对实验结果无影响;
d.读取数据时仰视读数造成读取的二氧化碳体积偏大,导致测定结果偏大;
e.稀硫酸加入烧瓶占据体积造成二氧化碳体积偏大,导致测定结果偏大;
故填:ab。