题目内容
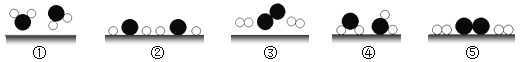
【题目】三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法错误的是( )
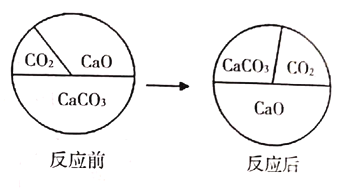
A.CaO为生成物
B.该反应是分解反应
C.反应后容器中固体质量减少
D.反应后容器中氧元素质量分数增大
【答案】D
【解析】
A、碳酸钙反应后质量减少,碳酸钙属于反应物,氧化钙反应后质量增加,属于生成物,二氧化碳反应后质量增加,属于生成物,不符合题意;
B、该反应符合“一变多”的特点,属于分解反应,不符合题意;
C、该反应是碳酸钙分解为氧化钙和二氧化碳,有二氧化碳气体生成,所以,反应后容器中固体质量减少,不符合题意;
D、根据质量守恒定律,化学反应前后,元素的质量不变,物质的总质量不变,故反应后容器中氧元素质量分数不变,符合题意。
故选D。

【题目】下表是四种常见的天然色素,回答下列问题:
名称 | 叶绿素b | 叶黄素 | 姜黄素 | 甜菜红 |
化学式 | C55H70MgN4O6 | C40H56O2 | C21 H20O6 | C24 H26N2O13 |
性质 | 不溶于水,可溶于乙醇等溶剂;稳定性不好,光、酸、碱、氧化剂等都能使其分解 | 不溶于水,易溶于油脂;耐热性能好,但对 光和氧不稳定 | 不溶于水,溶于乙醇;耐光性和耐热性较差 | 易溶于水,不溶于油脂;耐热性较差 |
(1)有机化合物中也可能含有金属元素,如叶绿素b中含有______________________________(填元素名称)元素。
(2)姜黄素中碳、氢、氧三种元素的原子个数比为______________________________。
(3)根据表中信息,可推测出保存甜菜红的方法是______________________________(写出一条即可)。
(4)计算叶黄素中氧元素的质量分数为______________________________(精确到0.1%)。
(5)绿色植物可利用体内的叶绿素通过光合作用将二氧化碳转化为氧气, 请指出该反应在人类生活中的重要作用:______________________________(写出一条即可)。