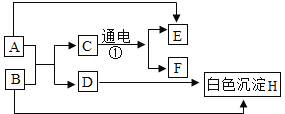
��Ŀ����
����Ŀ��ˮ�����౦�����Ȼ��Դ��
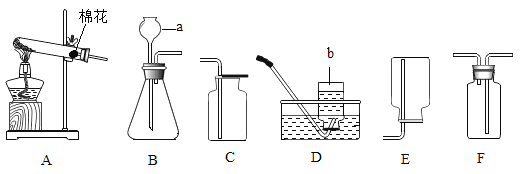
��1����Ȼˮ�к����������ʣ�ʵ���ҳ��ù��˷�����ȥˮ�в��������ʡ�������Ҫ�õ��������д���Ȧ������̨���ձ���©����________(����������)��
��2��Ӳˮ����������������ܶ��鷳�������г���________�ķ���������ˮ��Ӳ�ȡ�
��3����������������ˮ����������ʵ������ȡ�����Ļ�ѧ����ʽΪ:![]() ��X�Ļ�ѧʽΪ________��
��X�Ļ�ѧʽΪ________��
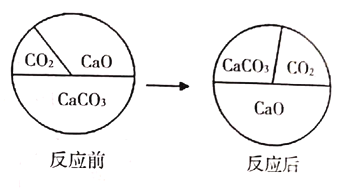
��4���ҹ���ѧ�������Ƴ�������Ч����������£�����̫���ֽܷ�ˮ��������ˮ��ͨ�����Ӵ���������ʱ,�ֽ���۹�����ʾ��ͼ��ʾ����(��O����ʾ��ԭ�ӣ���![]() ����ʾ��ԭ�ӣ���
����ʾ��ԭ�ӣ���![]() �� ��ʾ����)��
�� ��ʾ����)��
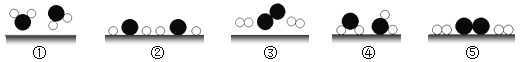
��ˮ�ֽ��۹��̵���ȷ˳����_______(�����)�����������У������ٷֵ�������_______����д���÷�Ӧ�Ļ�ѧ����ʽ:______��
��5���������ֹ������ʵ��ܽ��������ͼ��ʾ��
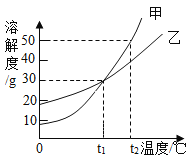
��t2��Cʱ�����ҵı�����Һ��100g,������Һ���ܼ���������С��ϵΪ:��______��(����>������="����<��)��
����t2��Cʱ150g�ı�����Һ������t1��C��������Һ�����ʵ���������Ϊ______(��������ȷ��0.1%)��
���𰸡������� ��� MnCl2 �٢ܢڢݢ� ��ԭ�Ӻ���ԭ��  < 23.1%
< 23.1%
��������
��1��������Ҫ�õ��������д���Ȧ������̨���ձ���©������������
��2�������г�����еķ���������ˮ��Ӳ�ȣ�
��3��![]() �����������غ㶨�ɣ���ѧ��Ӧǰ��ԭ�ӵ��������Ŀ���䣬��X�Ļ�ѧʽΪ��MnCl2��
�����������غ㶨�ɣ���ѧ��Ӧǰ��ԭ�ӵ��������Ŀ���䣬��X�Ļ�ѧʽΪ��MnCl2��
��4��ˮ�ֽ���۹���Ϊ��ˮ���ӷֽ�Ϊ��ԭ�Ӻ���ԭ�ӣ�ÿ������ԭ�ӽ�ϳ�һ������ӣ�ÿ������ԭ�ӽ�ϳ�һ�������ӣ���ˮ�ֽ��۹��̵���ȷ˳���Ǣ٢ܢڢݢۣ�
�ڻ�ѧ�仯�У����ӿ����ٷ֣�ԭ�Ӳ����ٷ֣��ʲ����ٷֵ���������ԭ�Ӻ���ԭ�ӣ�
ˮ�ڹ�����������·ֽ�Ϊ�������������仯ѧ��Ӧ����ʽΪ�� ��
��
��5����t2��Cʱ�����ܽ�ȴ����ҵ��ܽ�ȣ���t2��Cʱ�����ҵı�����Һ��100g�����������������ҵ������������ʼ��ܼ�����С���ҵ��ܼ����������<��
�ڼ��ܽ�����¶ȵ����߶����ӣ���t2��Cʱ150g�ı�����Һ������t1��C�����DZ�����Һ�� t1��Cʱ�����ܽ��Ϊ30g��������Һ�����ʵ���������Ϊ��![]() ��
��

����Ŀ������ʦ��ָ���£�С����С��������ͼ1��ʾװ�ö���������������������˵�̽��ѧϰ��
����:
������ص��۵�ԼΪ356��C���������̵ķֽ��¶�ԼΪ535��C���þƾ��Ƹ����ʼ���,�������ʵ��¶�һ��ԼΪ400��C����;
����ͬ�����ָ����غͶ������̻�����У�����غͶ������̵�������;
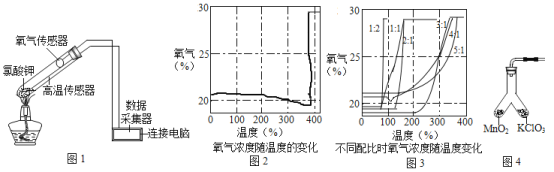
������طֽ�ʱ���������������Ũ�����¶ȵı仯ʾ��ͼ(ͼ2)����ͬ���ʱ����Ũ�����¶ȵı仯ʾ��ͼ(ͼ3)���¡�
��ش���������:
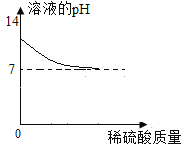
��1������ͼ2,����طֽ��¶�_____(������������������������������)���۵㡣
��2������ͼ2,������طֽ�ǰ���������������Ũ�Ƚ��͵Ŀ���ԭ����_________��
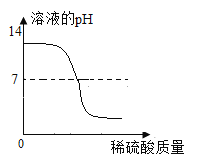
��3������ͼ3,����طֽ��¶���������ȱ仯�Ĺ�����_______��
��4��Ϊ֤ʵ�������̵Ĵ�����,С��������ͼ4װ�ý������±���ʾ��ʵ��:
���� | ʵ����� | ʵ������ | ʵ����� |
�� | ���װ�������� | ||
�� | �ֱ�����Y"�ι�����֧���м��������������̺�����أ�������Ƥ���� | û���������� | |
�� | �ֱ��þƾ����Ⱥ���ȶ�����������أ��ô�����ľ�����ڵ��ܿڡ� | �������֧�ܣ��ɹ۲� ��________�������Ҳ�֧�ܣ��ɹ۲쵽________�� | �����������Ȳ��ֽ�;��������Ƚϳ�ʱ���ֽ⡣ |
�� | ��ȴ��, ����Y�� �ι����֧���в��ֶ������̻����Ҳ�֧��:�У�����Y���ιܼ��ȣ��ô�����ľ�����ڵ��ܿڡ� | ����ʱ����벽����ľ���ܿ츴ȼ | �û�ѧ��ʽ��ʾ_______�� |
��ش�:
��������������
�ڲ���IV�У����������̻����Ҳ�֧�������ȵ�������еIJ���������_________��
��С����Ϊ���ݲ���IV��ʵ���������˵����������������طֽ�Ĵ�������С����ͬ�����Ĺ۵㣬С����Ϊ����֤���ڴ˷�Ӧ�ж������̵�______��_________���䡣��������ʦ��ָ���£�С��������ʵ�鷽��,������֤���Լ��Ľ��ۡ�
����Ŀ��ij��ѧ��ȤС����������ȡ�����Ĵ���չ��̽������ش���������:
̽��һ:��������������С�Դ�Ч����Ӱ��

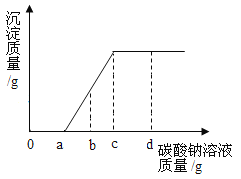
ȡ���ݵ���������أ��ֱ�����������������С��ͬ�Ķ������̽��м��ȣ��ô�������ù��������(��Ӧ��ʣ����������뷴Ӧǰ��������֮��)����ͼ:
(1)���������������������������ȡ�����Ļ�ѧ����ʽΪ_____________��
(2)�������ϵ�֪��������Ӧ���¶�Խ�ͣ���Ч��Խ�á�������ͼ,������طֽ��Ч�����õ���_____________����Ч�����õ�ԭ�������_____________��
̽����:������������������Դ�Ч����Ӱ��
ͬѧ���������ʵ�鷽��:
��� | ���������/g | ���� | ��������/g | �ռ�VmL���� ����ʱ��/s |
ʵ��1 | 5 | 171 | ||
ʵ��2 | 5 | �������� | 0.25 | 79 |
ʵ��3 | 5 | �������� | 0.5 | 49 |
ʵ��4 | 5 | �������� | 2.5 | 93 |
ʵ��5 | 5 | ������ | 0.5 | 58 |
ʵ��6 | 5 | �Ȼ��� | 0.5 | 154 |
(3)�����������ִ����У���Ч����õ���_____________��
(4)��������������ص�������Ϊ_____________ʱ����Ч����á�
(5)�Ȼ���_____________(����������������)�����á�ά�ּ����������䣬��ʵ��1�ټ����ռ�VmL����������ʱ����������171s,ԭ����_____________��
̽����:�������������ڷ�Ӧǰ��ı仯
ͬѧ�Ƿ���ÿ��������غͶ���������ȡ�����������ڲ�жװ��ʱ�����ŵ��̼�����ζ�����ǽ����Ⱥ�ʣ������еĶ������̷��벢������������������С�ڼ���ǰ�������̵��������������Ϻ��֣�һ����Ϊ��������غͶ������̻����ķ�Ӧ��������:
��1��: ![]() (����Cl2�д̼�����ζ)
(����Cl2�д̼�����ζ)
��2��: ![]()
��3��: ![]()
(6)��3����Ӧ����Ԫ�ػ��ϼ۱仯Ϊ_____��________��
(7)��Ӧ��ʣ������ж�����������С�ڷ�Ӧǰ��������ԭ�������_____________��