题目内容
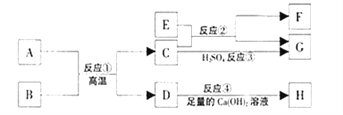
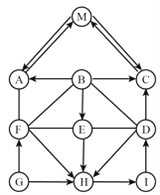
【题目】图中 A—M 是我们初中常见的化合物,是由 H、C、N、O、S、Cl、Ca 元素组 成的;M 为常见的有机物,A、C、G 为氧化物,且 G 中两种元素质量之比为 5:2,其中 E 为人体胃液中的主要成分。图中“——”表示两端的物质能发生化学反应;“→”表示物质间存 在的转化关系;反应条件、部分反应物和生成物略去。
(1)物质 E 的化学式为____________;M 的名称为____________。
(2)G→F 为_________ 反应(填放热或吸热)。
(3)B→E 的反应方程式为______________ 。
(4)E 和 D 反应的方程式为______________ 。
【答案】 HCl; 葡萄糖 放热 H2SO4+BaCl2=2HCl+BaSO4↓ 2HCl+CaCO3=CaCl2+CO2↑+H2O
【解析】图中 A—M 是我们初中常见的化合物,是由 H、C、N、O、S、Cl、Ca 元素组成的;M 为常见的有机物,A、C、G 为氧化物,且G中两种元素质量之比为 5:2,其中 E 为人体胃液中的主要成分,E是盐酸,M与A、C能相互转化,所以A、C是CO2、H2O,G 为氧化物,且G中两种元素质量之比为 5:2,所以G是CaO,F是氢氧化钙,A是H2O,C是CO2,M是葡萄糖,D是碳酸钙,B是硫酸,代入验证成立;(1)E是盐酸,化学式是HCl;M 的名称为葡萄糖;(2)G→F是氧化钙与水反应放出热量;(3)B→E是硫酸生成盐酸的反应方程式为:H2SO4+BaCl2=2HCl+BaSO4↓;(4)E和D反应的方程式为:2HCl+CaCO3=CaCl2+CO2↑+H2O。

 阅读快车系列答案
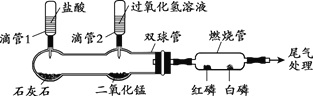
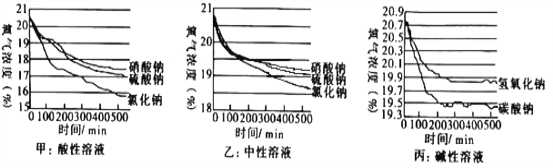
阅读快车系列答案【题目】利用下图装置完成A或B两个实验。请任选1个作答,若两题均作答,按A计分。(白磷的着火点为40℃,红磷的着火点为240℃)
A | B |
挤压滴管1,一段时间后,加热燃烧管至240℃以上。 (1)双球管中发生反应的化学方程式为_______。 (2)燃烧管中白磷和红磷均不燃烧,其原因是___________。 | 挤压滴管2,一段时间后,微热燃烧管至80℃。 (1)双球管中发生反应的化学方程式为___________。 (2)得出可燃物燃烧需要温度达到着火点的结论,对应的现象是___________。 |
| |
【题目】金属的性质
金属材料是现代生活和工农业生产中应用极为普遍的一类重要物质。请回答下列问题:
(1)请阅读以下信息,并将文中错误的描述标出:_______________ (填写序号)。
①金属都具有银白色金属光泽,②有良好的导电性和导热性。③汞是熔点最高的金属。④合金是由金属与其他金属或非金属熔合而成的,⑤合金是具有金属特性的纯净物,⑥合金一般比组成它的金属硬度大。
(2)大多数金属化学性质活泼,但活泼性有差异。例如,锌、铁、铝这三种金属与氧气或酸液等物质的反应的剧烈程度各有差异。请根据这三种金属的性质完成下面的表格。
反应现象描述 | 对应的金属 (化学式) | 构成该金属的粒子 (粒子符号) | 反应的化学方程式 | 基本反应类型 |
纯氧炉中火星四射 | _____ | _____ | _____ | _____ |
常温即形成致密氧化膜 | _____ | _____ | _____ | _____ |
与稀硫酸反应剧烈程度居中 | _____ | _____ | _____ | _____ |
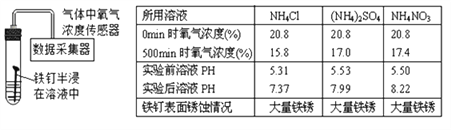
(3)大多数金属暴露在空气中都易被腐蚀,请举两条防止金属锈蚀的措施:①____________;②____________。
回收重新冶炼是保护金属资源的一条有效途径。请写出用一氧化碳在高温条件下还原锈蚀钢铁(主要成分是Fe2O3)的化学方程式:__________________。
但有时我们也会利用锈蚀为生活服务,请写出下列金属的应用原理:
① 食品袋中的铁粉 ②
食品袋中的铁粉 ② 暖贴中的铁粉 ③
暖贴中的铁粉 ③ 暖气片上涂的铝粉
暖气片上涂的铝粉
①___________________ ;②________ ;③________________ 。
(4)从金属的原子结构看,金属易与其它物质发生反应的根本原因是________________。