题目内容
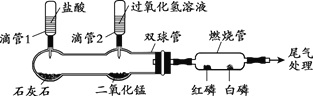
【题目】利用下图装置完成A或B两个实验。请任选1个作答,若两题均作答,按A计分。(白磷的着火点为40℃,红磷的着火点为240℃)
A | B |
挤压滴管1,一段时间后,加热燃烧管至240℃以上。 (1)双球管中发生反应的化学方程式为_______。 (2)燃烧管中白磷和红磷均不燃烧,其原因是___________。 | 挤压滴管2,一段时间后,微热燃烧管至80℃。 (1)双球管中发生反应的化学方程式为___________。 (2)得出可燃物燃烧需要温度达到着火点的结论,对应的现象是___________。 |
| |
【答案】 CaCO3+2HCl=== CaCl2+H2O+CO2↑ 可燃物没有与氧气接触 2H2O2![]() 2H2O + O2↑ 燃烧管中红磷不燃烧,白磷燃烧
2H2O + O2↑ 燃烧管中红磷不燃烧,白磷燃烧
【解析】A.(1)石灰石主要成分是碳酸钙,滴加盐酸后,双球管中发生反应的化学方程式为:CaCO3+2HCl=== CaCl2+H2O+CO2↑(2)燃烧管中是二氧化碳气体,没有氧气支持燃烧,所以燃烧管中白磷和红磷均不燃烧。B.(1)在二氧化锰作催化剂的条件下,过氧化氢溶液发生分解反应生成水和氧气:2H2O2![]() 2H2O + O2↑。(2)燃烧管中的白磷燃烧,红磷不燃烧,说明燃烧需要温度达到着火点。是因为白磷的着火点是40℃,红磷的着火点是240℃,温度达到了白磷的着火点,而没有达到红磷的着火点。
2H2O + O2↑。(2)燃烧管中的白磷燃烧,红磷不燃烧,说明燃烧需要温度达到着火点。是因为白磷的着火点是40℃,红磷的着火点是240℃,温度达到了白磷的着火点,而没有达到红磷的着火点。

 阅读快车系列答案
阅读快车系列答案【题目】实验探究一:课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
实验步骤 | 实验现象 | 实验结论及解释 |
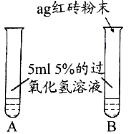
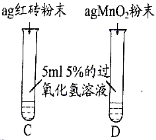
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是______ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡且______ | 红砖粉末的催化效果没有二氧化锰粉末好 |
【拓展应用】
己知CuSO4也可作为过氧化氢分解的催化剂。向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气_____g。
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究。
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质。写出KOH变质的化学方程式为_____。
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想_____不成立。
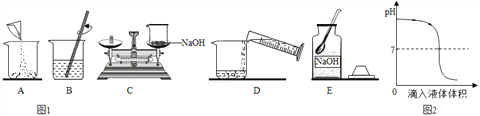
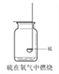
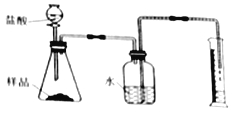
(2)准确称取一定质量的固体样品,放在右图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由_________。
(3)请你另外设计一个方案,进一步探究变质情况
实验步骤 | 实验现象 | 实验结论 |
猜想2成立 |
【题目】绿矾(FeSO47H2O)用途广泛,可用作净水剂,医学上可用作补血剂,还可用于制颜料。
(1)绿矾是一种絮凝剂,利用其溶于水后生成的胶状物对杂质的____________,使杂质沉降来达到净水的目的。
(2)缺铁会引起贫血,铁是一种人体必需的__________(填“常量元素”或“微量元素”)。
(3)《本草纲目》中记载,绿矾“煅过变赤,则为绛矾”。绛矾是古代壁画、彩塑中使用的一种红色颜料。
某化学兴趣小组同学对绿矾高温分解的产物很感兴趣,进行了如下探究。
(查阅资料)
①绿矾高温分解的产物是一种固态金属氧化物和几种气态非金属氧化物。
②在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低。
③无水硫酸铜遇水变蓝。
④硫有两种常见的氧化物,部分性质如下表:
硫的氧化物 | 熔点 | 沸点 | 水溶性 | 能否使高锰酸钾溶液褪色 |
SO2 | -75.5℃ | -10℃ | 易溶于水 | 能 |
SO3 | 16.8℃ | 44.8℃ | 易溶于水 | 不能 |
(提出问题)
《本草纲目》中记载绿矾“煅过变赤”,经实验验证绿矾高温分解确实产生红色固体,说明绿矾高温分解产生的一种固态金属氧化物是____________,那么产生的几种气态非金属氧化物是什么呢?
(进行猜想)猜想1:H2O 和____________;
猜想2:H2O 和SO3 ;
猜想3:H2O、SO2和SO3 。
甲同学认为无需通过进一步实验即可判定猜想2错误,理由是_______________________。
(设计实验)
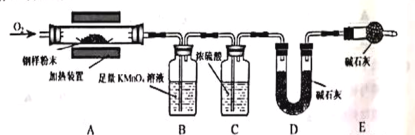
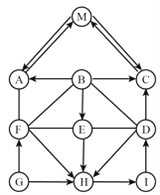
乙同学用以下装置检验绿矾高温分解产生的气态非金属氧化物:
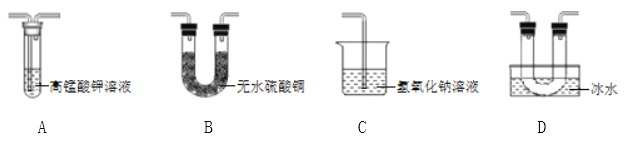
需将绿矾高温分解产生的气体依次通过______________(填字母,且每套装置限用一次)。
(分析现象)进行上述实验,观察到A中试管内溶液________,B中U形管内固体________,D中U形管内出现无色晶体,说明猜想3正确。
(得出结论)绿矾高温分解的化学方程式为_______________________________________。
(拓展延伸)生产硫酸最古老的方法是使绿矾高温分解,将生成的SO3和H2O同时冷凝并发生反应SO3+H2O=H2SO4 ,所以古代称硫酸为“绿矾油”。假定SO3和H2O全部冷凝并充分反应,SO2全部逸出,则通过这个方法得到的硫酸的质量分数为____________(计算结果保留一位小数)。
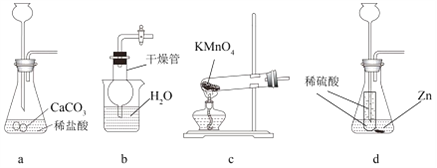
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是
A | B | C | D | |
实 验 装 置 |
|
|
|
|
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化测出减少的O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 烧杯中的水:加热铜片;隔绝空气 |
A. A B. B C. C D. D