题目内容
【题目】每年的 CES(国际消费类电子产品展览会)都会有一大波“黑科技”产品发布, 而这些产品大多是由金属材料制成,铜是其中重要的金属材料。
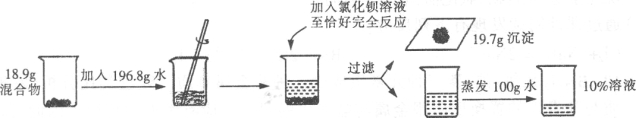
I.自然界中的铜主要以化合物形式存在于铜矿石中,从“绿色化学”的理念分析,以下铜矿最适宜炼铜的是_____(填序号)
A 黄铜矿(CuFeS2) B 辉铜矿(Cu2S)
C 蓝铜矿 [Cu(OH)2(CO3)2 ] D 斑铜矿(Cu5FeS4)
II.某化学兴趣小组用如下实验装置制取一氧化碳,再用一氧化碳还原氧化铜模拟炼铜。
(查阅资料)
(1)实验室常用甲酸(H2CO2)和浓硫酸混合加热制备 CO,同时生成 H2O。
(2)浓硫酸具有吸水性。
(进行实验)小组同学组装好下图装置并检查装置气密性之后开始实验,先让 A 装置反应一会儿,然后熄灭 A 中的酒精灯,再点燃 C 装置中的酒精灯。
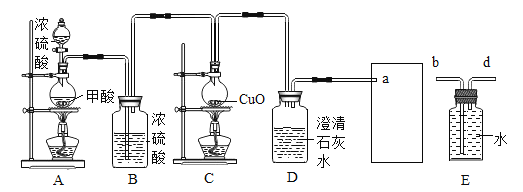
(1)装置 B 的作用是_____;装置 C 中发生反应的化学方程式是_____。
(2)装置 D 的作用是_____;该装置的组装存在的错误是_____; 改正之后,该装置中发生反应的化学方程式是_____。
(3)为避免一氧化碳污染空气,回收利用一氧化碳,方框中应连接装置 E,与 a 导管接口相接的是_____(填“b”或“d”)。
(4)实验结束之后,得到带有金属光泽的砖红色粉末,小组决定对该固体的成分进行探究。
(提出问题)红色的固体是什么?
(查阅资料)氧化亚铜(Cu2O)是红色粉末状固体;
会与稀硫酸反应:Cu2O + H2SO4 == CuSO4 + Cu + H2O。
(提出猜想)猜想一:该固体全部为 Cu;
猜想二:该固体全部为 Cu2O;
猜想三:该固体为 Cu2O 和 Cu 的混合物。
(实验方案)
实验步骤 | 实验现象及实验结论 |
取少量固体粉末于试管中, 加入过量_____溶液。 | 若无明显变化,则猜想一成立; 若溶液变为_____色,则猜想二或猜想三成立。 |
为了进一步确定混合物的组成,另取 m g 固体,重复上述实验,然后将反应后的物质过滤、洗涤、干燥,再次称量得到 n g 固体,若 m 和 n 满足_____的量的关系,则 猜想三成立。
(得出结论)该固体为 Cu2O 和 Cu 的混合物。
(交流讨论)
(1)从实验安全的角度考虑,本实验存在的危险是_____,改进的方法是_____;
(2)从物质的转化程度考虑,小组同学针对如何将氧化铜全部转化为铜单质展开讨论, 查阅了大量资料之后知道,反应条件是影响生成物的重要因素,因此一致认为在下次实验中需要适当加大 CO 的通入量或者_____。
【答案】C 干燥生成的一氧化碳 ![]() 检验是否生成二氧化碳 D装置中的左导管应该伸入澄清石灰水中 Ca(OH)2+CO2=CaCO3↓+H2O d 稀硫酸 蓝 n>
检验是否生成二氧化碳 D装置中的左导管应该伸入澄清石灰水中 Ca(OH)2+CO2=CaCO3↓+H2O d 稀硫酸 蓝 n>![]() m 缺少尾气处理装置 在实验的尾部添加一盏酒精灯 控制反应的温度
m 缺少尾气处理装置 在实验的尾部添加一盏酒精灯 控制反应的温度
【解析】
Ⅰ:A、B、D三种矿石中都含有硫元素,在冶炼的过程中,硫元素会转化为二氧化硫污染大气。所以从绿色化学的角度分析,从源头上杜绝污染,所以最适宜冶炼的矿石是C。故答案为:C;
Ⅱ:(1)浓硫酸和甲酸在加热的条件下反应生成一氧化碳和水。B中的浓硫酸可以干燥生成的一氧化碳,防止实验危险的发生。生成的一氧化碳和C中的氧化铜反应生成铜和二氧化碳。故答案为:干燥生成的一氧化碳、![]() ;
;
(2)装置D盛放的是澄清的石灰水,可以检测C中是否生成二氧化碳。该装置中,应该将左侧的导管伸入到集气瓶的药品液面下方。氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水。故答案为:检验是否生成二氧化碳、D装置中的左导管应该伸入澄清石灰水中、Ca(OH)2+CO2=CaCO3↓+H2O;
(3)为避免CO污染空气,回收利用一氧化碳,用排水法将生成的一氧化碳收集起来。气体应该从短管进入,水从长管流出。故答案为:d;
[实验方案]:根据题干信息可知,因为铜和稀硫酸不反应,氧化亚铜和稀硫酸反应生成硫酸通,能观察到溶液由无色变为蓝色。所以可以取少量固体粉末于试管中,加入过量的稀硫酸。若观察到溶液不变色,则证明固体全为铜。若观察到溶液变蓝色,则证明固体含有氧化亚铜,即猜想二或猜想三成立。若mg的红色固体全是氧化亚铜,则设生成的铜的质量为x。
 。
。
解得x=![]() g。所以若全是氧化亚铜,则生成的铜的质量为
g。所以若全是氧化亚铜,则生成的铜的质量为![]() g。若是红色固体中含有铜,则反应生成铜的质量小于
g。若是红色固体中含有铜,则反应生成铜的质量小于![]() g,所以若得到的固体的质量n>
g,所以若得到的固体的质量n>![]() g,则红色固体中含有铜。故答案为:稀硫酸、蓝、n>
g,则红色固体中含有铜。故答案为:稀硫酸、蓝、n>![]() ;
;
[交流讨论](1)该实验中需要一氧化碳还原氧化铜,一氧化碳有毒而且是一种大气污染物,需要增添一种尾气处理装置。一氧化碳具有可燃性,可以在装置的尾部增添一盏酒精灯,避免大气污染。故答案为:缺少尾气处理装置、在实验的尾部添加一盏酒精灯;
(2)根据题干可知,一氧化碳还原氧化铜生成铜和二氧化碳。但是在温度不同的条件下,生成的产物可能不是铜而是氧化亚铜。所以在实验室,为了将氧化铜全部转化为铜,应该控制反应温度或通入大量的一氧化碳。故答案为:控制反应的温度。

【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
[演示实验]将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____。
[查阅资料] CaC12溶液显中性
[提出问题]实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
[猜想与假设]针对疑问,甲组同学猜想如下:
猜想I:只有CaC12
猜想II:有_____
猜想III:有CaC12和Ca (OH)2
猜想IV:有CaCl2、HC1 和Ca (OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_____。
[实验探究]为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | _____ | _____ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca (OH)2 | 溶液中含有Ca (OH)2 | 溶液中含有Ca (OH)2 |
[得出结论]通过探究,全班同学一致确定猜想III是正确的。
[评价反思]
(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca (OH)2,请你帮助他们说明原因_____。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_____。