题目内容
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图所示。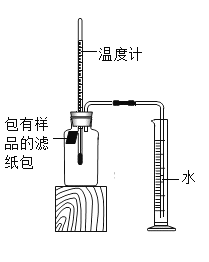
观察到量筒内水沿导管慢慢进入广口瓶(净容积为146ml,当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如表.
序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | 1g铁粉.0.2g碳,10滴水和少量NaCl | 100 | 70 | 约70 |
3 |
(1)实验①和②说明NaCl可以______(填“加快”或“减慢”)铁绣蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_______(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是______。
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成。______
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是______%(保留3位有效数字)。
【答案】加快 放热 Fe2O3 1g铁粉、10滴水 20.5%
【解析】
实验①和②说明NaCl能加快铁锈蚀的速率,铁和氧气和水共同作用生成铁锈。
(1)实验①和②之间唯一的变量为是否有NaCl,根据含有NaCl的②组实验,反应所需的时间较短,得到NaCl能加快铁锈蚀的速率。
(2)通过温度升高,可以直接得出铁锈蚀的过程是放热的过程。
(3)铁和氧气和水共同作用生成铁锈,可以判定此物质为铁锈,主要成分为Fe2O3。
(4)“实验①和③是探究碳对铁锈蚀速率的影响”,所以该对照组间唯一的变量应为是否含有碳,因为实验①还有碳,则实验③不含碳,而其它的因素应完全相同,所以实验③的样品组成为1g铁粉、10滴水。
(5)量筒内液体减少的体积即为广口瓶内所含有的全部氧气的体积,所以氧气的体积含量是![]() 。
。

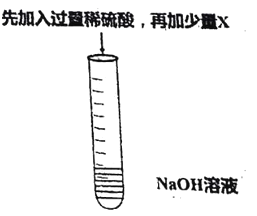
【题目】某化学学习小组在学习常见的盐的性质后,完成了如下实验。该学习小组对废液杯上层清液的溶质的成分进行了探究。请完成以下探究过程,并将答案填入空白相应位置。
(提出问题)上层清液中含有什么溶质?
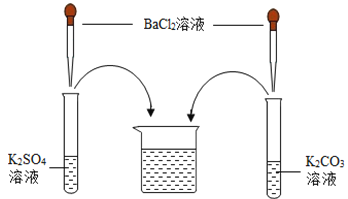
(作出猜想)Ⅰ溶质仅为_____(填化学式);Ⅱ溶质为KCl和BaCl2;Ⅲ溶质为KCl和_____(填化学式);Ⅳ溶质为KCl和K2CO3;Ⅴ溶质为KCl、K2SO4和K2CO3;Ⅵ溶质为KCl、K2SO4、BaCl2和K2CO3。
(交流讨论)小强同学认为猜想Ⅵ一定是错误的,他的理由是_____。
(设计方案)
实验操作 | 现象 | 结论 | |
取少量废液缸中上层清液,分装于甲、乙两支试管中 | 先向甲试管中滴加盐酸至过量 | 无明显现象 | 猜想Ⅳ、Ⅴ不正确 |
再向乙试管中滴加_____溶液(填化学式) | _____ | 猜想Ⅱ正确 | |
(交流反思)学习小组经过讨论认为:实验过程中无须使用AgNO3溶液,其理由是_____(用文字表述)。
【题目】为了测定某铜锌合金中铜的质量分数,某同学利用该合金与稀盐酸反应,进行了三次实验,有关实验数据记录如下(实验中的误差忽略不计)。
第一次 | 第二次 | 第三次 | |
所取合金的质量/g | 25 | 25 | 50 |
所用稀盐酸的质量/g | 120 | 160 | 100 |
生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
(1)分析表格数据可知,合金与所用稀盐酸的质量比为_____时,合金中的锌与稀盐酸中的HCl 恰好完全反应。
(2)试计算该铜锌合金中铜的质量分数_____。
【题目】根据金属的化学性质并结合表中信息,填写下表空白。
反应物 | 反应规律 | 反应规律的应用举例 |
金属+O2 | 大多数金属能和O2反应生成金属氧化物 | 铝表面形成一层致密薄膜阻止铝进一步氧化,该薄膜的化学式为________ |
金属+酸 | 在金属活动性顺序里,位于氢前面的金属能与盐酸、稀硫酸发生置换反应,生成盐和H2 | 写出用稀硫酸鉴别黄金和黄铜(铜锌合金) 的化学方程式______ |
金属+盐 | 在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们的盐溶液里置换出来,生成_____ | 用Cu、Mg、Zn中的两种金属分别放 入_____溶液中,即可比较出上述三种金属的活动性强弱 |