��Ŀ����
����Ŀ���Ķ�������Ϣ���ϣ����ش�������⣺
��������ѧʽΪ![]() �����³�ѹ��Ϊ����ɫ����ǿ�Ҵ̼�����ζ���ж����壬�ܶȱȿ���������ˮ����ѹ������Һ��Ϊ���ɫҺ̬�ա������л���������Ϊ5%���ϵ�����ʱ����ǿ��ᷢ�����ҵĻ�ѧ��Ӧ�����Ȼ������壬�ų�������ʹ���弱�����ͣ�������ɱ�ը��Σ�գ�����������������Ծ���ȼ�գ����������İ��̣�ͬʱ�ų����������������ڳ���Ϊ��ֽ����֯��ҵ��Ư������������ͨ��ˮ�У�������
�����³�ѹ��Ϊ����ɫ����ǿ�Ҵ̼�����ζ���ж����壬�ܶȱȿ���������ˮ����ѹ������Һ��Ϊ���ɫҺ̬�ա������л���������Ϊ5%���ϵ�����ʱ����ǿ��ᷢ�����ҵĻ�ѧ��Ӧ�����Ȼ������壬�ų�������ʹ���弱�����ͣ�������ɱ�ը��Σ�գ�����������������Ծ���ȼ�գ����������İ��̣�ͬʱ�ų����������������ڳ���Ϊ��ֽ����֯��ҵ��Ư������������ͨ��ˮ�У�������![]() ��
��![]() �������ᣩ���������������ɱ�������ã���������Ҳ����������ˮ������
�������ᣩ���������������ɱ�������ã���������Ҳ����������ˮ������
��1����������Ҫ����������_________________��
��2���������������ȼ�գ������ġ����̡���________________��
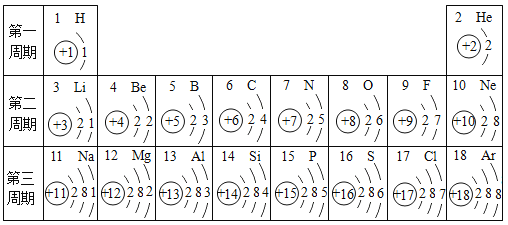
��3��![]() �������ᣩ����Ԫ�صĻ��ϼ���________________��
�������ᣩ����Ԫ�صĻ��ϼ���________________��
��4��������������Ӧ�����ֱ���ʽΪ��_________________��
���𰸡����³�ѹ��Ϊ����ɫ����ǿ�Ҵ̼�����ζ�����壬�ܶȱȿ���������ˮ����ѹ������Һ��Ϊ���ɫҺ̬�� �Ȼ��ƹ���С���� ![]()
![]()
��������
��1����������Ҫ���������У����³�ѹ��Ϊ����ɫ����ǿ�Ҵ̼�����ζ�����壬�ܶȱȿ���������ˮ����ѹ������Һ��Ϊ���ɫҺ̬�ȣ�
��2���������������ȼ�յķ�Ӧԭ����2Na��Cl2![]() 2NaCl�����������������ǣ��Ȼ��ƹ���С����;
2NaCl�����������������ǣ��Ȼ��ƹ���С����;
��3��![]() �������ᣩ�У���Ԫ����+1�ۣ���Ԫ����-2�ۣ�����Ԫ�ػ��ϼ�Ϊx�����У���+1��+x+��-2��=0����x=+1����Ԫ�صĻ��ϼ��ǣ�+1�ۣ�
�������ᣩ�У���Ԫ����+1�ۣ���Ԫ����-2�ۣ�����Ԫ�ػ��ϼ�Ϊx�����У���+1��+x+��-2��=0����x=+1����Ԫ�صĻ��ϼ��ǣ�+1�ۣ�
��4��������������Ӧ�����Ȼ��⣬��Ӧ�����ֱ���ʽΪ������+����![]() �Ȼ��⡣
�Ȼ��⡣

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��MnSO4H2O�ڹ�ҵ��ũҵ�ȷ����й㷺��Ӧ�á�
��һ���Ʊ�����ҵ���û�����β���е�Ũ��SO2�����̿���Ҫ�ɷ�MnO2�����ʽ���Ԫ��Mg��Al��Fe�ȣ��Ʊ�MnSO4H2O�������£�
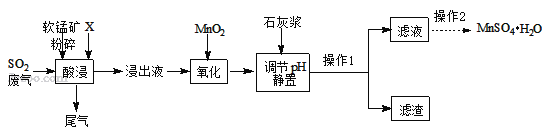
��֪������Һ����������Ҫ��H+��Mn2+��Mg2+��Fe2+��Al3+�ȣ����������з�������Ҫ��Ӧ��ѧ����ʽΪ��MnO2+SO2=MnSO4��
��1�������н����̿�����Ŀ����____��
��2������X���ѡ��_____��
a.���� b.���� c.����
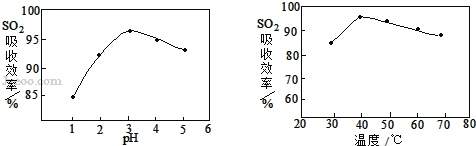
��3�����ʱSO2������Ч����pH���¶ȵĹ�ϵ����ͼ��ʾ��Ϊ���SO2������Ч�ʣ����ʱpH������____���ң��¶ȿ�����_________�����������ˡ�
��4���������������������Ŀ���ǽ�Fe2+ ����ΪFe3+�������Ʒ�Ӧ�Ļ�ѧ����ʽMnO2+2FeSO4+_______ = MnSO4 + Fe2(SO4)3 + 2H2O����
��5������ʯ�ҽ�����pH���ɽ�������Ľ���Һ�����������γ����������ȥ��
��֪����һ���й������������pH��Ӧ��
�������� | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Mg(OH)2 |
��ʼ����pH | 1.8 | 4.1 | 8.3 | 9.4 |
��ȫ����pH | 3.2 | 5.0 | 9.8 | 12.4 |
������Fe3+����KSCN��Һ������Ѫ��ɫ���ʯ�ҽ�ʱӦ������Һ��pH��ΧΪ_________���ⶨ��Һ��pH���ѡ____��a.pH��ֽ b.pH�ƣ�������Fe3+�Ƿ��������ѷ�����________��
��6������1�������˺�ϴ�ӣ������õ��IJ����������ձ�����������_____��ϴ�ӵ�Ŀ����________
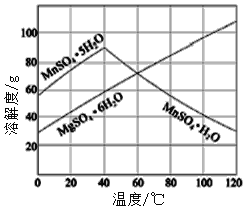
��7����֪�����̡�����þ�ᾧˮ������ܽ��������ͼ�������2����������Ũ����___________�����ˡ�ϴ�ӡ����
������Ӧ�ã�
��8����MnSO4�ɲⶨˮ���ܽ����������ǣ�ȡ100mL ˮ����Ѹ�ټ�������MnSO4��Һ������NaOH��KI��Һ�������������ӡ���ʹ֮��ַ�Ӧ�������ӣ�Ѹ�ټ���������ϡ���ᣬ��ʱ��I2���ɣ�����0.79gL��1Na2S2O3��Һ��I2��Ӧ��������Na2S2O3��Һ 12.0mLʱ��Ӧ��ȫ���йػ�ѧ��Ӧ����ʽ�£�
��2MnSO4+O2+4NaOH=2MnO(OH)2+2Na2SO4��
��MnO(OH)2 + 2KI + 2H2SO4 = MnSO4 + K2SO4 + I2 + 3H2O��
��I2 + 2Na2S2O3 = Na2S4O6 + 2NaI��
����ˮ�����ܽ�����Ũ�ȣ���mgL-1Ϊ��λ����д���������________��