题目内容
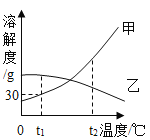
【题目】质量相等的两个烧杯中装入等质量的锌粉和铁粉,再分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如19题图所示,下列说法错误的有( )
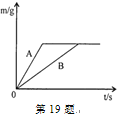
①A表示锌和稀硫酸的反应曲线
②反应结束后两种金属一定都有剩余
③两份溶液中的硫酸一定都反应完
④反应掉的锌和铁的质量比为56:65
⑤反应结束后消耗两种金属的质量相等
⑥反应结束后两烧杯中物质的质量相等
A.2个B.3个C.4个D.5个
【答案】B
【解析】
①锌的活动性比铁的活动性强,等质量的金属,锌反应的时间短,正确;
②根据化学方程式Fe+H2SO4═FeSO4+H2↑,可知每56g铁生成2g氢气,根据化学方程式Zn+H2SO4═ZnSO4+H2↑,可知每65g锌反应生成2g氢气;由方程式分析可知,二者反应结束后,生成相等质量的氢气消耗的金属的质量不相等,由图示生成的氢气相等,故稀硫酸完全反应,可能金属都有剩余,也可能锌恰好反应完,铁有剩余,错误;
③置换反应是金属置换酸中的氢元素,所以若生成的氢气的质量相等,硫酸均反应完,正确;
④由图象可知,生成的氢气的质量相等,由以上分析可知,所需锌和铁的质量比为65:56,错误;
⑤由方程式分析可知,二者反应结束后,生成相等质量的氢气消耗的金属的质量不相等,错误;
⑥质量相等的两个烧杯中装入等质量的锌粉和铁粉,再分别放入质量相等、溶质质量分数相同的稀硫酸中,最终生成的氢气质量也相等,所以反应结束后两烧杯中物质的质量相等,正确。说法错误的有3个。
故选B。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】下列化学知识归纳整理的相关内容中完全正确的一组是:
A.数轴表示 | B.化学巨匠及杰出贡献 |
① ② | ①张青莲--测量相对原子质量 ②侯德榜--发明联合制盐法 |
C.实验操作的先后顺序 | D.化学元素与人体健康 |
①点燃可燃性气体——先验纯后点燃 ②CO还原CuO——先加热后通入CO | ①缺铁元素--会引起贫血 ②缺碘元素--会引起甲状腺肿大 |
A.AB.BC.CD.D
【题目】小军家的下水管道堵了,爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了。小军对此很好奇,于是想探究“管道通”中的物质成分。
(提出问题)“管道通”中的物质是什么?
(查阅资料)主要内容如下:
(1)下水管道里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉为银灰色固体,铝粉与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是____
②铝与氢氧化钠溶液反应的化学方程式是:2A1+2NaOH+2H2O=2NaAlO2+3H2↑。
(猜想与验证)小军打开一盒“管道通”,内有袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
实验操作 | 实验现象 |
①将几粒白色固体颗粒放在表面皿上,放置一会儿 | ______ |
②将适量白色固体颗粒放人盛有适量水的试管中,并用手触摸试管外壁 | 试管外壁发烫 |
③向步骤②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银灰色粉末为铝粉。
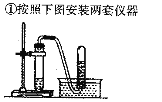
实验操作 | 实验现象 |
| |
②一套仪器中加入银灰色粉末和稀盐酸;另一套仪器中加入银灰色粉末和______ | 都产生大量无色气体,试管外壁温度明显升高 |
③待导管口有气泡均匀持续冒出时,分别收集1试管气体,验纯 | 用拇指堵住试管口,移近酒精灯火焰,松开拇指,____ |
④在导管口点燃气体 | 火焰颜色为____ |
(结论)银灰色粉末为铝粉。
(反思)①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似。要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在;
②根据本实验分析,使用“管道通”时,应注意的事项有____(填一条即可)。