题目内容
【题目】某钙片的标签如下,且知此钙片成分中只有碳酸钙CaCO3含有钙元素。

(1)高钙片中的“钙”应理解为 ___________(填序号)
①元素 ②原子 ③分子 ④单质
(2)维生素种类较多,其中维生素D2的化学式为C28H44O,则维生素D2的相对分子质量为_________,维生素D2中C、H、O三种元素的原子个数之比为______
(3)如果一个青少年每天需要补钙0.8克,其中0.6克都来自于牛奶,其余服用钙片。请计算每天他需要补充碳酸钙多少克?(要求有计算过程)________
【答案】① 396 28:44:1 0.5g
【解析】
解:(1)高钙片中的“钙”不是以单质、氧化物、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关;
(2)C28H44O的相对分子质量=12×28+1×44+16=396;维生素D2中C、H、O三种元素的原子个数之比为28:44:1;
(3)一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片,则每天从钙片中补充钙元素的质量为:0.8g-0.6g=0.2g;碳酸钙中钙元素的质量分数为40/100×100%=40%,每天他需补充碳酸钙的质量为0.2g÷40%=0.5g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实 验 装 置 |
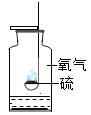
硫在氧气中燃烧 |
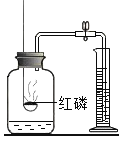
测定空气中氧气含量 |
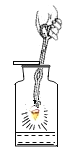
铁丝在氧气中燃烧 |
排水法收集氢气 (氢气难溶于水) |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察氢气何时收集满 |
A.AB.BC.CD.D
【题目】某学生为了探究甲烷的组成元素,设计并完成了如下探究实验,请你帮他完成下面的实验报告:
提出问题:甲烷中含有哪些元素?
(查阅资料)含碳元素的物质完全燃烧生成![]() 。
。
实验探究:
实验步骤 | 实验现象 | 解释与结论 |
①在空气中点燃甲烷, ②将洁净干燥的小烧杯罩在甲烷燃烧的火焰上方。 | 烧杯内壁有水珠。 | 证明生成物有水,甲烷中一定含有_______元素。 |
③将蘸有澄清石灰水的小烧杯罩在甲烷燃烧的火焰上方。 | _____________。 | 证明生成物有 |
(1)表达与交流:经实验测定甲烷的化学式为![]() ,请你写出甲烷燃烧方程式:________________。
,请你写出甲烷燃烧方程式:________________。