题目内容
【题目】通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
20℃时,一些物质的溶解度 | ||
OH﹣ | CO32﹣ | |
Na+ | 溶 | 溶 |
Ca2+ | 微 | 不 |
Mg2+ | 不 | 微 |
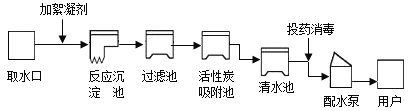
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验.
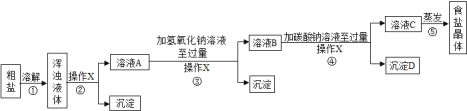
[交流与表达]
(1)实验操作X的名称是__,该操作中要用到的玻璃仪器有烧杯、玻璃棒和__.
(2)实验步骤③的主要目的是__ (用化学方程式回答);
(3)实验步骤④中生成的沉淀D是__.
[反思与评价]
(4)有同学认为原实验方案不完善,为了完善原实验方案,你设计的实验是_______。(写出补充部分的实验操作和现象)
【答案】过滤 漏斗 MgC12+2NaOH=2NaCl+Mg(OH)2↓ CaCO3 第五步蒸发前先向溶液中加稀盐酸至PH=7
【解析】
(1)操作X是固液分离的步骤,故是过滤。过滤中用到的玻璃仪器有烧杯、玻璃棒、漏斗。
(2)原溶液中的氯化镁可以与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,故该步骤的目的除去氯化镁,反应的方程式为:MgC12+2NaOH=2NaCl+Mg(OH)2↓。
(3)步骤4是氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,故填碳酸钙。
(4)由题干分析可知,溶液C中含有的溶质有碳酸钠和氯化钠,故要加入稀盐酸除去碳酸钠。

 同步奥数系列答案
同步奥数系列答案【题目】定性和定量是研究化学实验的两种方法,我们可以通过观察某个实验现象来定性认识,也可以通过称量化学反应前后的质量变化来定量研究。通常瓦斯气体可能含有CO、CO2、CH4等气体,某兴趣小组为确定该气体是否含有这三种气体中的一种或几种,初步设计了如下实验方案供大家讨论:
已知:CH4在加热条件下会与氧化铜反应生成铜、二氧化碳和水。
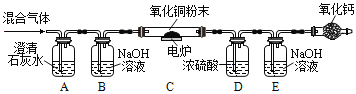
(1)实验过程若发现A处澄清石灰水变浑浊,发生的化学方程式为_____。
(2)同学甲认为,氧化钙的作用是防止空气中的_____对实验造成干扰,小组成员一致同意。
(3)同学乙认为,若装置C中CuO变红,则除了甲烷与CuO可能发生反应外,还可能发生的反应是_____;(用化学方程式表示)。
(4)装置B中装有足量NaOH溶液,其作用是: _____。
(5)同学丙认为,欲通过D装置中浓硫酸因吸收水分而增重,说明混合气体中含有CH4的思路不严密,认为需要在_____ (填序号) 间再增加一个装有_____的洗气瓶 (编号为F),才能证明含有CH4。
(6)同学丁认为该装置存在着重大安全隐患,理由是_____。综合上述讨论,兴趣小组将经过处理后的混合气体,通过改进后的装置进行了实验探究,请根据实验现象和数据填写结论:
装置 | 实验现象/数据 | 实验结论 |
A | 石灰水变浑浊 | 通过实验现象和数据,小组成员一致认为该气体样品中含有_____。 |
B | 无明显现象 | |
C | 黑色粉末变成红色 | |
D | 装置D增重1.8g | |
E | 装置E增重2.2g |
【题目】将一定量的丙烷(C3H8)和氧气置于一个密闭的容器中引燃并充分反应,测得反应前后各物质的质量如表所示,下列判断不正确的是( )
物质 | C3H8 | O2 | H2O | CO2 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
A.表中a的值一定是5.6
B.若8.8g丙烷完全反应,则生成14.4g水
C.生成物X中一定含有氢元素
D.若4.4g丙烷与16.0g氧气充分反应,则无X生成