题目内容
取一定量的木炭在一定量的氧气中燃烧,生成23.2g气体(氧气已完全反应).将生成的气体通入过量的澄清石灰水中,生成40g沉淀.试通过计算分析23.2g气体的成分和质量. g .
CO2 17.6g,CO 5.6g
试题分析:根据二氧化碳会与氢氧化钙生成碳酸钙沉淀,依据碳酸钙的质量可以求出二氧化碳的质量,再根据混合气的质量求出一氧化碳的质量.
解:设生成40g的沉淀需要二氧化碳的质量为X,
CO2+Ca(OH)2=CaCO3↓+H2O
44 100
x 40g
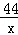 =
=
x=17.6g,
所以二氧化碳为17.6g,一氧化碳质量为:23.2g﹣17.6g=5.6g,
故答案为:CO2 17.6g,CO 5.6g
点评:在解此类题时,首先分析题中反应涉及的原理,然后原理写出方程式,再根据方程式中的比例关系求出相关的数据.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目