题目内容
【题目】在A+B![]() C+D的反应中,下列叙述错误的是
C+D的反应中,下列叙述错误的是
A. 若C和D为盐和水,该反应不一定是中和反应
B. 若A是氧化铜、C为铜,该反应不一定是置换反应
C. 若将20gA和30gB混合,则生成C和D的总质量一定为50g
D. 此反应可能是复分解反应
【答案】C
【解析】
A、生成盐和水的反应不一定是中和反应,例如氧化铁可以和盐酸反应生成氯化铁和水,其中氯化铁为盐,但是氧化铁不是碱,该反应不是中和反应,不符合题意;
B、置换反应是指单质和化合物反应生成另一种单质和另一种化合物的反应,氧化铜和氢气反应生成铜和水,该反应为置换反应,氧化铜和一氧化碳反应生成铜和二氧化碳,而一氧化碳和氧化铜都是化合物,该反应不是置换反应,不符合题意;
C、根据质量守恒定律:参加化学反应的各物质的质量总和,等于反应后生成各物质的质量总和。因为不知道20gA和30gB混合是否恰好完全反应,所以生成C和D的总质量不一定为50g,符合题意;
D、复分解反应是指两种化合物交换成分生成另外两种化合物的反应,所以题中所给反应可能为复分解反应,不符合题意。故选C。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案【题目】下表为氯化钠、碳酸钠在水中的溶解度。我国西北地区有很多咸水湖,其中最大的是柴达木盆地的察尔汗盐池。某盐湖附近的农民通过“冬天捞碱.夏天晒盐”获得大量湖盐。这里的“碱”指纯碱(主要成分是碳酸钠) ,盐指氯化钠。
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度 | 氯化钠 | 35.7 | 35.8 | 35.9 | 36.1 | 37.1 |
碳酸钠 | 7.0 | 12.5 | 21.5 | 39.7 | 49.0 | |
(1)请据图表简要解释“冬天捞碱,夏天晒盐”其中的道理____。
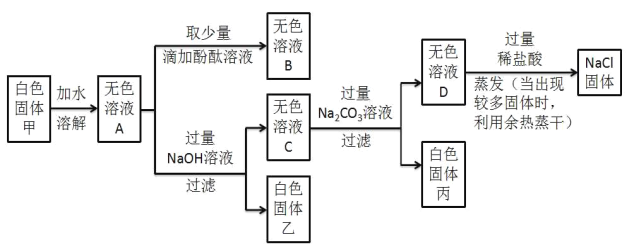
(2)小勤同学取该湖盐样品进行探究。
(提出问题)该湖盐样品的成分是什么?
(猜想与假设)猜想一:只有Na2CO3:猜想二:只有NaCl;猜想三:Na2CO3和NaCl。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量样品于试管中,向其中加入足量的____溶液;过滤,得沉淀和滤液,向沉淀中加入足量稀硝酸 | 产生白色沉淀 部分白色沉淀消失 | 猜想三成立 |
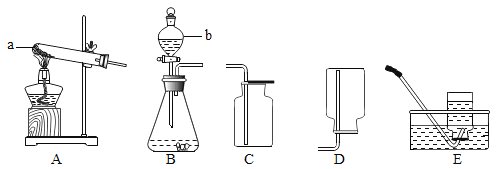
(拓展延伸)为进一步确定该湖盐样品中Na2CO3的质量分数,小勤同学再取该湖盐样品10.00g做了如图所示的补充实验(假定每步均完全反应或吸收)。

①反应结束之后通入足量空气的目的是_____。
②装置A中氢氧化钠溶液的作用是_____(用化学方程式表示)。
③实验结束后测得装置E增重0.44g,请根据上图所示的实验过程和提供的数据计算该湖盐样品中碳酸钠的质量分数是多少_____?(写出计算步骤,计算结果精确到0.1%)
【题目】将一定量的乙醇(C2H6O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
下列判断正确的是( )
A. 表中a的值为2.6
B. X一定是该反应的催化剂
C. X可能含有氢元素
D. 若起始时氧气的质量是9.6g,则无X生成
【题目】为比较4种金属X、Y、Z、W的活动性,小刚进行了一系列实验,结果如表所示![]() 其中能反应的记为“
其中能反应的记为“![]() ”,不能反应的记为“
”,不能反应的记为“![]() ”,无标记的表示未做该实验.则它们的金属活动性顺序为
”,无标记的表示未做该实验.则它们的金属活动性顺序为![]()
参加反应的物质 | X | Y | Z | W |
|
|
|
| |
|
|
| ||
稀盐酸 |
|
|
|
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()