题目内容
【题目】将一定量的乙醇(C2H6O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
下列判断正确的是( )
A. 表中a的值为2.6
B. X一定是该反应的催化剂
C. X可能含有氢元素
D. 若起始时氧气的质量是9.6g,则无X生成
【答案】D
【解析】
A、由表中数据分析可知,反应前后,乙醇的质量减少了4.6g,故乙醇是反应物,参加反应的乙醇的质量为4.6g;同理可以确定氧气是反应物,参加反应的氧气的质量为8.0g;水是生成物,生成的水的质量为5.4g;生成二氧化碳的质量为4.4g;由质量守恒定律,X应是生成物,且生成的X的质量为4.6g+8.0g﹣5.4g﹣4.4g=2.8g,故表中a的值为0g+2.8g=2.8g,故选项说法错误;
B、由A选项分析可知,X的质量增加,故一定不是该反应的催化剂,故选项说法错误;
C、根据反应前后元素质量不变,反应物乙醇中含氢元素的质量为4.6g×![]() ×100%=0.6g,生成物水中含氢元素的质量为5.4g×
×100%=0.6g,生成物水中含氢元素的质量为5.4g×![]() ×100%=0.6g,氢元素的质量相等,故X中不含氢元素,故选项说法错误;
×100%=0.6g,氢元素的质量相等,故X中不含氢元素,故选项说法错误;
D、由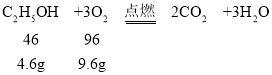 可知,4.6克乙醇能与9.6克的氧气恰好完全反应,生成了二氧化碳和水,故选项说法正确。
可知,4.6克乙醇能与9.6克的氧气恰好完全反应,生成了二氧化碳和水,故选项说法正确。
故选D。

 名校课堂系列答案
名校课堂系列答案【题目】石灰石是生产石灰、水泥的主要原料。某研究性学习小组为测定当地石灰石中碳酸钙的貭量分数,采取方法如下:取12g石灰石样品加入烧杯中,将120g稀盐酸平均分四次加入,充分反应后(已知石灰石中的杂质不溶于水也不与稀盐酸反应),测得剩余固体的质量记录如下:
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸的质量/g | 30 | 30 | 30 | 30 |
剩余固体的质量/g | 9 | 6 | 3 | 2 |
分析数据计算(结果精确到0.1%):
(1)12g样品中含碳酸钙的质量为多少______?
(2) 所用稀盐酸的溶质质量分数为多少______?
(3)12g样品中的碳酸钙恰好完全反应后,所得溶液的溶质质量分数为少______?
【题目】已知氧化铜还原成铜的过程中有氧化亚铜生成。如图是小华同学用CO还原氧化铜的实验装置图,当玻璃管中黑色物质全部变红后,小华想知道红色物质中有哪些成分?请你与小华一起完成下面的探究。
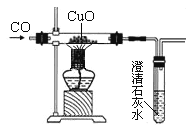
【提出猜想】①全部是铜; ②全部是氧化亚铜;③是铜和氧化亚铜的混合物。
【查阅资料】氧化亚铜是一种红色固体,能与稀硫酸发生如下反应:
Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验】为了验证这些猜想,小华同学进行了以下探究活动,请完成下列问题:
步骤 | 现象或数据 | 结论 |
(1)称取14.4g反应生成的红色固体于试管中,向其中加入足量的稀硫酸; | 现象:_______; | 猜想①错误 |
(2)将步骤(1)反应后的物质进行过滤,称量干燥后的固体质量为m。 | 数据: 若m = 6.4g; | ________ |
数据:若m_______6.4g (填:>、<或=)。 | 猜想③正确 |
【交流反思】(1)小华实验装置中的石灰水的主要作用是______________________________,从环保角度看,该装置有待改进,请写出一种改进措施_____________________________。
(2)请写出氧化铜与CO反应生成氧化亚铜的化学方程式_________________________。