题目内容
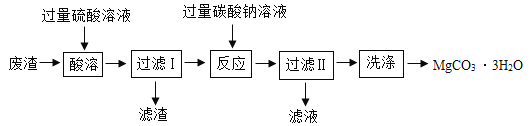
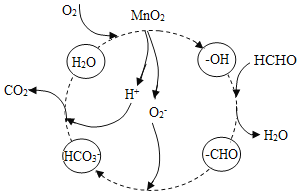
【题目】与以下四个变化过程对应的四个图象中,错误的是( )

A.一定量的饱和石灰水中加入一定量的氧化钙,溶液质量与加入后时间的关系
B.向pH=1的溶液中加水
C.两杯等质量足量的稀硫酸中分别加入等质量的镁、铝,溶液质量与时间的关系
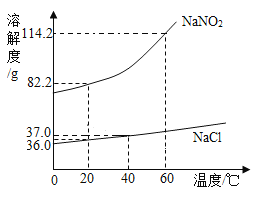
D.t℃时,在一定量的氯化钠不饱和溶液中不断加入氯化钠固体
【答案】D
【解析】
A、氧化钙与水反应生成氢氧化钙,放出大量的热,氢氧化钙的溶解度随温度的升高而降低,反应后由于温度升高、氧化钙与饱和溶液中的水发生反应而使溶液质量减少,反应后冷却至室温,溶液的质量增大,饱和溶液的溶剂减少会造成溶质析出,则溶液的溶质、溶剂都在减少,溶液的质量也在减少,故A正确;
B、向pH=1的溶液中加水,溶液的酸性逐渐减弱,pH变大。随着水的添加,溶液的pH会无限趋近于7,但是pH不会等于或大于7,故B正确;
C、设镁、铝的质量均为![]() ,与足量的稀硫酸反应后溶液质量增加分别为
,与足量的稀硫酸反应后溶液质量增加分别为![]() 。
。
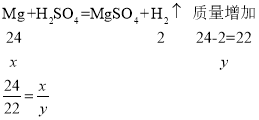
解得![]()
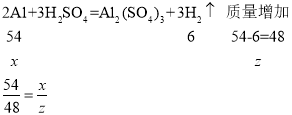
解得![]()
所以将等质量的金属镁和金属铝分别和质量分数相等的足量的稀硫酸混合,反应溶液增加的质量,镁大于铝。镁的活动性大于铝,镁反应速率较快,故C正确;
D、温度不变,则固体物质的溶解度不变,所以t℃时,在一定量的氯化钠不饱和溶液中不断加入氯化钠固体,氯化钠的溶解度始终不变,故D错误。故选D。

【题目】化学课上老师演示在氢氧化钠溶液中滴加稀盐酸实验时,出现了有气泡产生的现象,同学们计划对产生该现象的原因进行探究。
(提出问题)产生的气体成分是什么?
(设计实验)将生成的气体通入澄清的石灰水,石灰水变浑浊。
(分析与讨论)①生成的气体是_____。
②氢氧化钠已变质,变质的原因用化学方程式表示为_____。
(进一步探究)氢氧化钠溶液变质的程度如何?
(实验方案)
方案1:取少量氢氧化钠溶液的样品于一洁净试管中,先滴加酚酞溶液,酚酞变红色,再滴加氯化钙溶液,出现白色沉淀。
方案2:取少量氢氧化钠溶液的样品于一洁净试管中,先滴加澄清石灰水,出现白色沉淀,静置,再在上层溶液中滴加酚酞溶液,酚酞变红色。
(分析与讨论)同学们认为以上两个方案都不正确。
方案1不正确的原因是_____。
方案2不正确的原因是_____。
经过讨论同学设计了以下方案,得到了合理的结论。
实验步骤 | 实验现象 | 实验结论 |
(1)取少量氢氧化钠溶液的样品于一洁净试管中,先滴加过量的氯化钙溶液,观察现象。 | _____ | 氢氧化钠部分变质 |
(2)再向其中滴几滴酚酞溶液。 | 酚酞变红色。 |
实验中滴加过量氯化钙溶液的目的是_____。
在氢氧化钠溶液中滴加稀盐酸,溶液温度与滴加稀盐酸质量之间的变化关系如图所示:
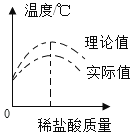
(1)实验中发现稀盐酸质量为m1时,测得的溶液温度最高,从能量的角度分析,氢氧化钠与稀盐酸的反应是_____反应;从反应进行的程度分析,温度达到最大值时,表示_____。随后溶液温度降低的原因是_____。
(2)实验数据分析可知测得的实际值低于理论值,请写出一点导致这种差异出现的原因_____。
【题目】在一只烧杯中进行如图实验,补全实验报告:
序号 | 目的 | 步骤 | 现象与结论 |
① | 探究_______ | I 加入5mL1%NaOH稀溶液 II 滴加2滴酚酞试液 III 逐滴加入1%稀盐酸并搅拌 | 酚酞的作用是_______ |
② | 检验NaOH已变质 | I 加入少量样品 II 加入适量水溶液 III 加入_______ | 现象是_____ |
③ | 验证KCl不能无限溶解 | I 20℃时加入50g水 II 加入10gKCl并搅拌 III 至少加入_______ (已知:20℃,SKCl=34g/100g水) |