题目内容
【题目】在一只烧杯中进行如图实验,补全实验报告:
序号 | 目的 | 步骤 | 现象与结论 |
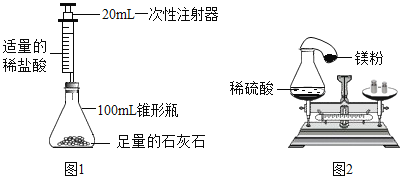
① | 探究_______ | I 加入5mL1%NaOH稀溶液 II 滴加2滴酚酞试液 III 逐滴加入1%稀盐酸并搅拌 | 酚酞的作用是_______ |
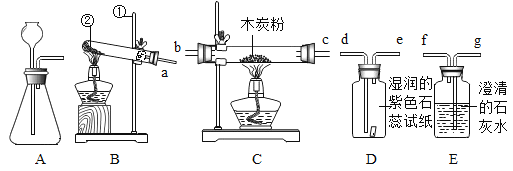
② | 检验NaOH已变质 | I 加入少量样品 II 加入适量水溶液 III 加入_______ | 现象是_____ |
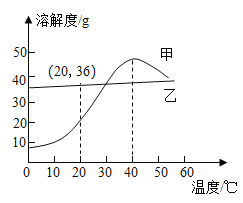
③ | 验证KCl不能无限溶解 | I 20℃时加入50g水 II 加入10gKCl并搅拌 III 至少加入_______ (已知:20℃,SKCl=34g/100g水) |
【答案】NaOH是否能与HCl中和反应 通过颜色变化判断反应发生 足量稀盐酸(合理即可) 产生气泡 大于7gKCl
【解析】
①氢氧化钠和盐酸反应生成氯化钠和水,该反应无明显现象,加入酚酞可使现象明显,从而证明发生了反应;故填:NaOH是否能与HCl中和反应;通过颜色变化判断反映发生。
②NaOH变质的原因是与空气中的二氧化碳反应生成了碳酸钠和水,只要检验样品中是否有碳酸钠存在即可,检验碳酸钠的存在可用稀盐酸,稀盐酸和碳酸钠反应生成氯化钠、水以及二氧化碳,只要变质了加入足量稀盐酸就会看见有气泡产生,故填:足量稀盐酸;产生气泡。
③20℃时,KCl的溶解度为34g/100g水,可知100g水中最多可以溶解34g的氯化钾,所以在50g水中加入10g的氯化钾后,再加入超过7g的氯化钾,固体没有完全溶解,可知氯化钾不能无限溶解;故填:大于7gKCl。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目