题目内容
【题目】无焰食品加热器常用于野外加热食物,它的成分是镁粉、铁粉、氯化钠。使用时加入水,镁与水反应产生热量。下面是在18℃、标准大气压的环境中对该产品的实验研究,请结合以下实验方案回答有关问题(不考虑氯化钠对水沸点的影响)。
实验1:
Ⅰ、将一定质量的镁条、铁粉和氯化钠加入盛有100mL水的隔热容器中,连续搅拌,每50s记录一次温度,得图1中曲线a;
Ⅱ、将相同质量的镁条剪成100份代替Ⅰ中镁条重复以上实验,得图1中曲线b;
Ⅲ、用相同质量的镁粉代替Ⅰ中镁条重复以上实验,得图1中曲线c。

(1)从能量变化角度看,该变化是_________能转化为_________能。
(2)观察图1,从中可以发现影响镁和水反应速率的因素_______。
实验2:将2.40g镁粉和质量为28.00g的铁粉混合,加入盛有100mL水的隔热容器中,不断搅拌。氯化钠用量不同时,温度变化情况如图2所示。
(3)实验2中,当NaCl质量大于7.30g时,实验不再做的原因是_______。
A.加入更多的NaCl不再增加反应速率
B.加入更多的NaCl会降低反应速率
C.已达到水的沸点,温度不会再有变化
D.需加入更多的铁粉来提高水的温度
(4)如果在实验2中加入质量为3.65gNaCl,混合物的温度最高大约是__________。
(5)某同学设计了下面四种无焰食品加热器物料配方,请根据本次实验研究的结论,判断其中最合理的是_________。
A. 2.40g镁粉、7.30g NaCl和28.00g铁粉
B.2.40g镁条、7.30g NaCl和28.00g铁粉
C. 2.40g镁粉、8.76g NaCl和28.00g铁粉
D.2.40g镁条、8.76g NaCl和28.00g铁粉
理由是_______________。
【答案】化学 热 镁的反应表面积(或镁的颗粒大小) C 40-50℃之间 A 镁粉比镁条能更快产生热量,配方A中已达到水的沸点,配方C中多余的NaCl造成原料浪费
【解析】
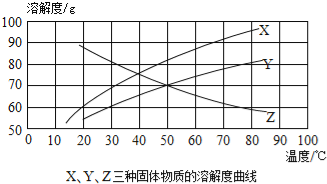
(1)根据图1曲线可知,金属镁与水反应放出热量,从能量变化角度看,该变化是化学能转化为热能;
(2)根据图1可知,相同的时间内,实验Ⅲ中水的温度上升最快,所以镁粉与水反应放出的热量最多,不难看出镁的反应表面积越大反应速度越快,温度变化较大。观察图1,从中可以发现影响镁和水反应速率的因素是镁的反应表面积(或镁的颗粒大小);
(3)根据图2图像可知当氯化钠的量为7.30g时液体沸腾,已达到水的沸点,温度不会再有变化,故选C;
(4)根据图2图像可知,如果在实验2中加入质量为3.65gNaCl,混合物的温度最高大约是40-50℃之间;
(5)镁粉比镁条能更快产生热量,在镁和铁质量相等的情况下,7.30g NaCl能使水达到沸腾。故选A;理由是镁粉比镁条能更快产生热量,配方A中已达到水的沸点,配方C中多余的NaCl造成原料浪费。