题目内容
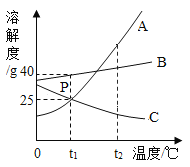
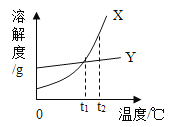
【题目】X、Y两种固体物质的溶解度曲线如图所示。下列说法正确的是_____
A两种物质的溶解度X>Y
B t2℃时,两种物质的饱和溶液中溶质的质量分数X>Y
C将t1℃时Y的饱和溶液升温至t2℃,溶质的质量分数增大
D若X中混有少量的Y,提纯X宜采用的方法是_____
【答案】B 降温结晶
【解析】
A、根据图像可知,当温度小于t1℃时,Y物质的溶解度大于X物质。A错误;
B、t2℃时,X物质的溶解度大于Y物质,因此两种物质的饱和溶液中溶质的质量分数X>Y。B正确;
C、将t1℃时Y的饱和溶液升温至t2℃,Y物质的溶解度增大,但溶液中Y物质的质量没有增加,溶剂质量也没有发生改变,因此溶质的质量分数与原溶液相比不发生改变。C错误;
D、X中混有少量的Y,则需要提纯X物质。X物质的溶解度受温度影响变化较大,则应该选用降温结晶的方法。
故答案为:B、降温结晶。

【题目】某同学为探究纯金属及其合金性质,进行了如下实验。
0-1小时 | 1 小时-2小时 | 2小时-3小时 | |
5%的稀硫酸 | 无气泡产生 | ||
15%的稀硫酸 | 无气泡 | 少量小气泡,反应缓慢 | 少量小气泡增加不明显,缓慢 |
表:黄铜片与不同浓度的稀硫酸
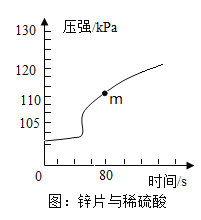
(1)取锌片于密闭容器中,加入足量5%的稀硫酸,反应时气体压强的变化曲线如图。开始时容器内气体压强几乎不变,共原因是_____________。 m点时,所得溶液中除水之外还含有的物质有______________。
(2)另取两片相同的黄铜(铜锌合金,含锌量与实验1相同),分别放入足量不同浓度的稀硫酸中,观察记录实验现象如表。分析可知,制成合金的一个目的是_____________。
(3)某工厂废液池中溶液的主要成分是硫酸锌、硫酸铜和硫酸,生产过程中还回收了一些锌粉。若只利用废液和锌粉制铜,请设计实验方案_____________。