题目内容
【题目】水是一种宝贵的资源。
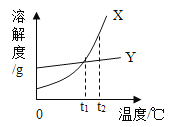
(1)水净化过程中活性炭的作用是_________,区别硬水和软水可用___________。 家中常用_______的方法降低水的硬度。
(2)水电解的化学方程式为_________________,说明水是由_______________组成的。
【答案】吸附 肥皂水 煮沸 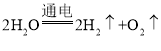 氢元素和氧元素
氢元素和氧元素
【解析】
(1)活性炭具有吸附性,可以吸附水中的色素和异味,故水净化过程中活性炭的作用是吸附;
可用肥皂水区分硬水和软水,肥皂水在硬水中泡沫较多,在软水中易起浮渣;
生活中常用煮沸的方法降低水的硬度;
(2)水在通电的情况下分解为氢气和氧气,该反应的化学方程式为: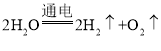 ;
;
化学反应前后,元素的种类不变,该实验可说明水是由氢元素和氧元素组成。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是( )
选项 | 实验目的 | 实验过程 |
① | 证明变质 | 取少量溶液,滴加足量盐酸,将生成的气体通入澄清石灰水 |
② | 确定成分 | 取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
③ | 测定纯度 | 取一定量溶液,加入盐酸,用氢氧化钠固体吸收生成的气体,称量 |
④ | 除去杂质 | 取溶液,滴加石灰水至恰好完全反应,过滤 |
A.②③B.①③C.②④D.①④
【题目】镀铬金属既漂亮又耐腐蚀,为了解金属铬的相关性质同学们进行了如下探究活动。
[查阅资料]
资料1:铬是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。
资料2:铬在发生置换反应时生成Cr2+,含有Cr2+的溶液常显蓝色。
[实验药品]铝片、铬片、铜片、稀硫酸、稀盐酸、CrSO4 溶液。
[实验过程]
(1)彬彬同学取大小相同的铝片、铬片和铜片,准备浸入到盛有相同质量分数的稀硫酸的三根试管中观察现象,三种金属片放入稀硫酸前要进行预处理是_____。
记录现象如下:
试管1 | 试管2 | 试管3 | |
实验现象 | 金属片表面产生气泡缓慢,溶液逐渐变蓝色 | 金属片表面产生气泡较快 | |
实验结论 | 三种金属的金属活动性由强到弱的顺序为_____。( 填元素符号) | ||
写出试管1中发生反应的化学方程式_____。
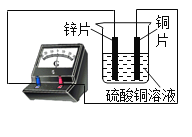
(2)明明从上面给定的实验药品中选了三种药品进行实验,也得出了上述三种金属的活动性强弱,则他选用的三种实验药品是_____,实验中发生反应的化学方程式为_____。
[学以致用]
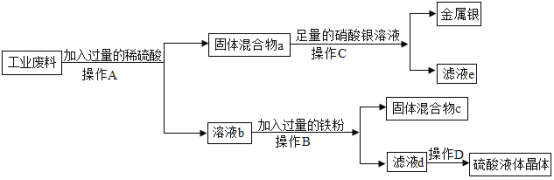
(3)彬彬同学了解到某电镀厂废水中含有AgNO3、Cu(NO3)2 和Cr(NO3)2,为了从中回收贵重金属银和一种盐晶体,他设计如下图实验流程:
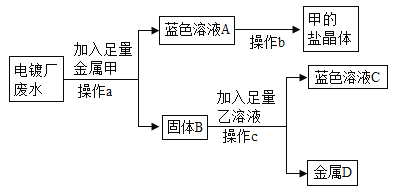
请回答:操作a加入足量的金属甲为_____,反应前固体B质量_____(填“大于”、 “小于”或“等于”)反应后固体D的质量。
[知识拓展]
(4)工业上可利用“铝热反应”来冶炼铬,其原理是在高温下用铝将铬从其氧化物(Cr2O)中置换出来。若要制得780kg铬,理论上至少需要铝的质量是多少_____?
【题目】将一段去除氧化镁的镁条放入一定量的盐酸中,有气泡产生,充分反应后静置,发现试管中有白色沉淀产生。为探究白色沉淀的成分,九(1)班兴趣小组同学在老师的指导下进行如下实验:
试管(盛有等体积等浓度的盐酸) | ① | ② | ③ | ④ |
镁条质量(g) | 1 | 1.5 | 2 | 2.5 |
实验现象 | 快速反应,试管发热,镁条全部消失 | |||
白色沉淀量(恢复至20°C) | 无 | 少量 | 较多 | 很多 |
(1) 4支试管中盛有等体积等浓度的盐酸的原因___________________。
[得出结论]
(2)镁条与盐酸反应产生白色沉淀的量与_________________有关。
[提出问题]
白色沉淀是什么物质?
[查阅资料]
在氯化镁溶液中,镁能与水常温下反应生成氢氧化镁和氢气。
[猜想与假设]
甲:白色沉淀可能是碳酸镁
乙:白色沉淀可能是生成的氯化镁增多析出的晶体
丙:白色沉淀可能是剩余的镁
丁:白色沉淀可能是氢氧化镁
(3)其他同学认为甲的猜想是错误的,原因是_________________。
[实验验证]
序号 | 操作步骤 | 实验现象 | 结论 |
1 | 取第一份白色不溶物于试管中,加入蒸馏水,震荡 | (4)沉淀____________溶解(选填会或不会) | 乙同学猜想不成立 |
2 | 取第二份白色不溶物于试管中,加入稀盐酸 | (5)___________________ | 丙同学猜想不成立 |
3 | ①取第三份白色不溶物于试管中,加入稀硝酸 ②向所得溶液加入几滴硝酸银溶液 | ①白色沉淀不溶解 ②出现大量白色沉淀 | ①丁同学猜想不成立 ②白色不溶物定含 (6)____________元素 |
[实验结论]
在老师的帮助下,同学们得出白色沉淀物是Mg2(OH)2Cl2,反应的化学方程式为2Mg+2HCl+2H2O=Mg2(OH)2Cl2+2H2![]() 。
。