题目内容
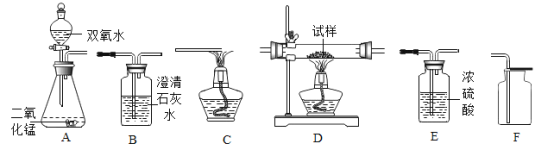
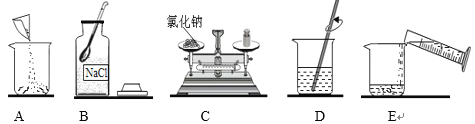
【题目】实验时,有同学不小心放错了胶头滴管,使得NaNO3溶液的试剂瓶中可能混入NaCl、NaOH、Na2CO3和 Na2SO4中的一种或几种。为了验证,他进行了如图所示的实验。
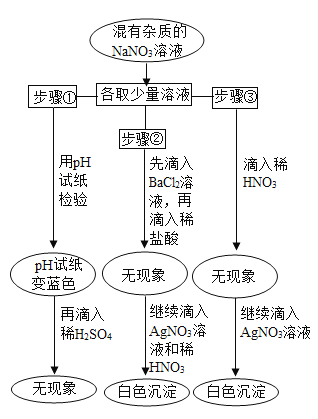
请回答:
(1)由步骤①得知,此溶液中含有(写化学式,下同)_____。
(2)由步骤②得知,此溶液中不存在_____。
(3)由步骤③得知,此溶液中含有_____。
【答案】NaOH Na2SO4和Na2CO3 NaCl
【解析】
解:(1)溶液使PH试纸变蓝色说明了溶液显碱性,滴入硫酸后无现象,说明了存在氢氧化钠,化学式为:NaOH;
(2)在实验室常用盐酸酸化的氯化钡检验硫酸根离子的存在,在步骤②中滴入盐酸酸化得氯化钡,无现象,说明了没有硫酸根离子也没有碳酸根离子,化学式为:Na2SO4和Na2CO3;
(3)在实验室常用硝酸酸化的硝酸银检验氯离子的存在,滴入硝酸无现象,排除了碳酸根离子,加入硝酸银生成沉淀,所有的硝酸盐都溶于水,就只有氯化银沉淀,此溶液中一定有氯化钠,化学式为:NaCl。

【题目】小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为15%.具体是什么物质无法辨认。老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种。
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是_____________
(2)小亮取少量样品于试管中,滴加______试液.试液变红色,该溶液不可能是_________,, (填写化学式),理由是________。
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告。
(设计实验方案)方案甲:选择氯化钙溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份。
(进行实验)你愿意选择方案_____ (选填“甲”或“乙”)进行实验。
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加 __________ | __________ | 该溶液是碳酸钠溶液。有关反应的化学方程式为: _____ |