题目内容
【题目】如图是初中化学的一些基本实验,请回答相关问题:
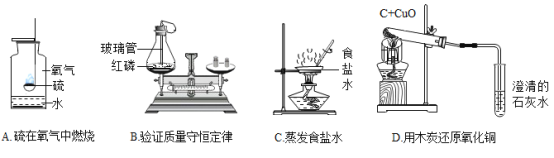
(1)A实验中集气瓶内水的作用是_____。
(2)B实验中气球的作用是_____。
(3)C实验过程中,当蒸发皿中出现_____时,停止加热。
(4)D实验的实验现象是_____。酒精灯网罩的作用是_____。
【答案】吸收二氧化硫,防止污染空气 防止气体逸出、调节装置内外压强平衡 出现较多固体 黑色粉末逐渐变红色,澄清的石灰水变浑浊 使火焰集中,提高温度
【解析】
(1)硫在氧气中燃烧生成有毒气体二氧化硫,A实验中集气瓶内水的作用是吸收二氧化硫,防止污染空气;
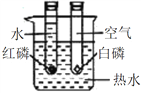
(2)验证质量守恒定律实验中,红磷燃烧放出大量的热,使装置内压强增大,气球的作用是防止气体逸出、调节装置内外压强平衡;
(3)蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干;
(4)碳具有还原性,与氧化铜在高温下反应生成铜和二氧化碳,D实验的实验现象是黑色粉末逐渐变红色,澄清的石灰水变浑浊。酒精灯网罩的作用是使火焰集中,使酒精燃烧充分,提高温度。

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案【题目】我国古代纺织业常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白织物。
(资料)①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 50 | |
溶解度/g | Ca(OH)2 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 |
K2CO3 | 107 | 109 | 110 | 114 | 121 | |
KOH | 97 | 103 | 112 | 126 | 140 | |
(1)20℃时,100 g 水中最多可溶解 K2CO3 的质量是__________g,溶质的质量分数为 50% 的 KOH 溶液属于 ___________溶液(填“饱和”或“不饱和”)。
(2)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,恢复到原温度,某些量随时间变化的关系如图所示。则纵坐标可能表示的是____________(填序号)
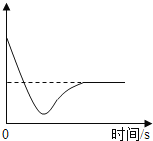
a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
(3)20℃时,将 1.38 g K2CO3 固体放入 100 g 水中,并加入一定量的氢氧化钙,搅拌使其充分反应,恢复到原温度,过滤,得到质量为 1.5 g 的固体。所得滤液中的溶质是____________,加入氢氧化钙的质量是_________g。
(4)将纯净的氯化钠配制成溶液。20℃时,向 4 个盛有 200 g 水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4 组实验数据如下:
实验序号 | ① | ② | ③ | ④ |
加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
溶液质量/g | 209 | 236 | 272 | 272 |
若将②中得到的溶液稀释成质量分数为 0.9%的生理盐水,需加水的质量是________g。关于上述实验的叙述正确的是__________(填序号)。
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体
【题目】戴口罩、勤洗手,给自己居住、生活的环境消消毒,都是预防新型冠状病毒感染的有效方法。其中“84”消毒液能用于日常生活的消毒灭菌。某化学兴趣小组对一瓶 敞口放置的“84”消毒液成分产生兴趣,在老师的指导下进行如下探究:
(提出问题)该敞口久置的“84”消毒液中含有哪些溶质?
(查阅资料)(1)“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO 为有效成分,有腐蚀性,并易与空气中 CO2 反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。
(2)次氯酸(HClO)溶液和次氯酸钠(NaClO)溶液都具有漂白、杀菌、消毒功效。
(3)HClO 不稳定,受热或光照易分解。
(提出猜想)I.“84”消毒液没有变质
II.____________
III.“84”消毒液完全变质
(设计方案)为验证猜想,设计如下方案:
实验操作 | 实验现象 | 结论 |
(1)另取该消毒液少量于试管中,滴加足量 BaCl2 溶液,振荡 | 产生白色沉淀 | 猜想________不成立,反应的化学方程式是____________。 |
(2)向盛有有色布条的烧杯中滴加该消毒液适量,放置一段时间 | 有色布条_________。(填“褪色”或“不褪色” | 猜想 II 不成立,猜想 III 成立 |
(得出结论)综上所述,该敞口放置的“84”消毒液中溶质一定有____________________。
(拓展延伸)
(1)次氯酸钠与盐酸反应会生成有毒的黄绿色气体单质,该气体单质是____________,因此,“84”消毒液____________________(填“能”或“不能”)与洁厕灵(主要成分为盐酸)混合使用。
(2)欲用 40%的 NaClO 溶液稀释配制 25%的溶液 400g,需要加水__________g。
【题目】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
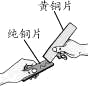
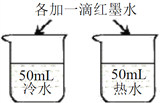
A | 探究温度对分子运动快慢的影响 |
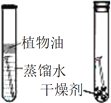
| B | 探究水对铁钉锈蚀的影响 |
|
C | 探究空气是燃烧的必要条件 |
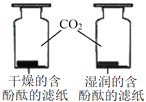
| D | 探究CO2与水反生反应 |
|
A. A B. B C. C D. D