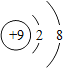题目内容
【题目】下列与化学有关的知识完全正确的一组是( )
A | ①鉴别硝酸铵和硫酸铵——加熟石灰研磨,闻气味 ②吃水果——可以补充维生素 ③墙内开花墙外香——分子不断运动 | B | ① ②Mg2+——“2”表示一个镁离子带2个单位正电荷 ③C1O2中氯元素的化合价+4价 |
C | ①食品包装填充氧气——防止变质 ②加碘食盐——补充碘元素 | D | ①活性炭净水——吸附色素和异味 ②常用水冲洗铁制品——防止铁生锈 ③硬水和软水——加肥皂水可以区分 |
A.AB.BC.CD.D
【答案】B
【解析】
A、①硝酸铵和硫酸铵中都含有铵根,加熟石灰研磨,铵根与氢氧根反应生成氨气,都会有刺激性气味,不能通过加熟石灰研磨,闻气味来鉴别硝酸铵和硫酸铵,说法错误;②水果中富含大量的维生素,吃水果可以补充维生素,说法正确;③墙内开花墙外香,是因为分子在不断运动,说法正确;A选项所涉及的化学知识有一个不正确,不符合题意;
B、①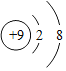 ,核电荷数为9,核外电子数比核电荷数多一个,微粒带一个单位的负电荷,因此表示的微粒符号为
,核电荷数为9,核外电子数比核电荷数多一个,微粒带一个单位的负电荷,因此表示的微粒符号为![]() ,说法正确;②“
,说法正确;②“![]() ”中的数字“2”表示一个镁离子带2个单位正电荷,说法正确;③C1O2中氧元素为-2价,根据化学式中元素化合价代数和为0可知氯元素的化合价为+4价,说法正确;B选项所涉及的化学知识完全正确,符合题意;
”中的数字“2”表示一个镁离子带2个单位正电荷,说法正确;③C1O2中氧元素为-2价,根据化学式中元素化合价代数和为0可知氯元素的化合价为+4价,说法正确;B选项所涉及的化学知识完全正确,符合题意;
C、①通常情况下食品包装填充氮气来防止变质,而不是氧气,说法错误;②加碘食盐中含有碘酸钾,可以补充碘元素,说法正确;C选项所涉及的化学知识有一个不正确,不符合题意;
D、①活性炭具有吸附性,利用活性炭吸附色素和异味来净水,说法正确;②常用水冲洗铁制品,不能防止铁生锈,铁制品上有水要擦干才能防止其生锈,说法错误;③肥皂水加入硬水中会有大量浮渣,泡沫少,肥皂水加入软水中浮渣少,泡沫多,硬水和软水加肥皂水可以区分,说法正确;D选项所涉及的化学知识有一个不正确,不符合题意。故选B。

 阅读快车系列答案
阅读快车系列答案【题目】回答下列问题。
(1)“侯氏制碱法”制备Na2CO3的流程如下。
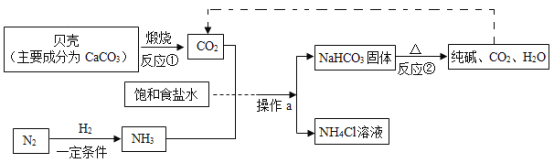
①反应②的化学方程式是___。
②操作a的名称是__,实验室进行此操作所需的主要玻璃仪器有烧杯、玻璃棒和____。
③流程图中能循环利用的物质是_(填化学式) ,副产品为_ ( 填化学式)。
(2)实验室制备纯碱( Na2CO3 )的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30~35°C,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。
四种盐在不同温度下的溶解度表( g/100g水)
温度 溶解度 | 0°C | 10° C | 20° C | 30° C | 40° C | 50° C | 60°C | 100°C |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 一 | 一 | 一 | 一 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 16.4 | 一 | |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①反应温度需要控制在30~ 35°C ,原因是__。为控制此温度,通常采取的加热方法为___。
②保温30分钟,静置后只析出NaHCO3晶体的原因__。
【题目】某化学研究小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中图1的实验,设计了图2的实验装置。
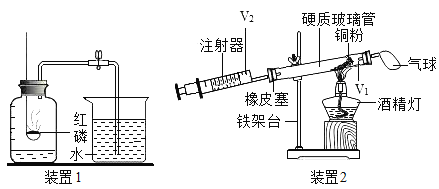
(1)A组同学用图1装置进行实验,红磷燃烧的现象是_____。实验后发现测得的氧气体积分数偏小,原因可能是_____。(填标号)
①红磷燃烧后,燃烧匙伸入不够迅速
②集气瓶没有冷却到室温就打开止水夹
③红磷的量太多
④实验前集气瓶里装水
⑤装置漏气
⑥红磷燃烧时,止水夹未夹紧
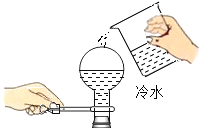
(2)B组同学用图2所示装置和药品进行实验,玻璃管容积V1为90mL,注射器的活塞实验前停在30mL处(V2为30mL),操作正确,得出氧气约占空气体积的五分之一,则注射器活塞最终停留在_____mL处,实验过程中,需缓慢推拉注射器活塞,目的是_____,若实验结束且冷却到室温后没有将气球内的气体全部挤出就读数计算,则测量结果会_____(填“偏大”或“偏小”或“不影响”)。
(3)C组同学用图1所示装置,将药品红磷换为木炭测定空气中氧气含量,若实验要成功则需将集气瓶内的水换成_____(填试剂名称)。该小组同学改用新方案进行实验,但发现结果始终偏小。
(提出问题)是什么原因导致测量不准确?
(猜想与假设)他们分别作如下猜想:
甲同学:可能是木炭的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
丙同学:可能是木炭与空气反应生成了其他气体。
(查阅资料)
木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达14.0%,8.0%和16.0%。
(探究一)小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,可知_____同学的猜想不成立。
(探究二)乙同学又利用上述装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验结论 |
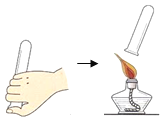
①将足量木炭点燃,迅速插入装有氧气的集气瓶中 | 木炭燃烧,发出白光,放热 | 乙同学猜想成立 |
②待装置冷却后,将燃着的_____(填“棉花”或“蜡烛”)再伸入集气瓶中 | _____ |
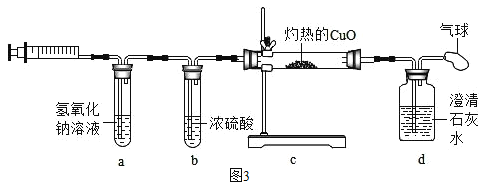
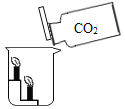
(探究三)丙同学从木炭燃烧产物的角度猜想还可能是生成了_____(填化学式)导致结果偏小;于是用注射器抽取集气瓶内的气体做了如图3所示的实验,气球的作用是_____,当观察到d中_____(填实验现象),可证明丙同学的猜想成立,则c中反应的化学方程式_____。