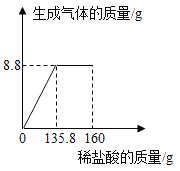
题目内容
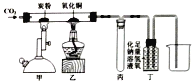
【题目】A为黑色固体,A、C、D、Y都是氧化物,E是单质,F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答:
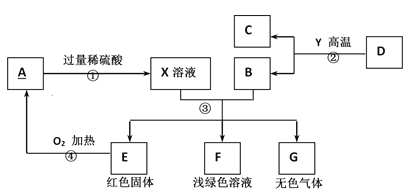
(1)X溶液中所含有的溶质为___,固体A的化学式为____________。
(2)写出反应③中生成无色气体的化学方程式_____。
(3)指出物质G和A在加热条件下发生的化学反应的基本反应类型是_____________________。
【答案】CuSO4和H2SO4 CuO Fe+H2SO4=FeSO4+H2↑ 置换反应
【解析】
E是单质且是红色固体,能与氧气在加热的条件下生成A这种氧化物,所以A是氧化铜,E是铜,氧化铜与过量的稀硫酸反应生成硫酸铜,所以X溶液中有硫酸铜和过量的稀硫酸,反应②是炼铁的主要反应,生成的B是单质,所以B是铁,由于生成的C是氧化物,所以C是二氧化碳,B与硫酸铜和稀硫酸都能反应,生成浅绿色的是硫酸亚铁,无色气体G是氢气,D和Y都是氧化物,所以无法确定一氧化碳,代入验证推理正确。所以:
(1)X溶液中所含有的溶质为CuSO4和H2SO4,固体A是氧化铜,化学式为CuO,故填:CuSO4和H2SO4 CuO;
(2)反应③中生成无色气体的化学方程式Fe+H2SO4=FeSO4+H2↑,故填:Fe+H2SO4=FeSO4+H2↑;
(3)物质G和A在加热条件下发生的化学反应是H2+CuO![]() Cu+H2O,这是单质与化合物生成单质和化合物的反应,故填:置换反应。
Cu+H2O,这是单质与化合物生成单质和化合物的反应,故填:置换反应。

【题目】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如下:
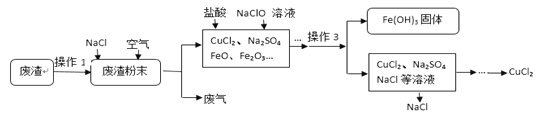
(1)操作1把废渣粉碎的目的 。
(2)在废渣粉末中加入NaCl和O2的目的是:CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4,写出该反应的化学方程式 。
(3)【查阅资料】:不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。下表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.9 | 4.7 |
沉淀完全的pH | 3.2 | 6.7 |
操作3的名称是 ,其中用到玻璃棒的作用是 。在此操作之前,为了使溶液中的Fe3+变成Fe(OH)3沉淀而除去,你认为调节溶液的pH到 (填数值范围)比较合适。
(4)流程图中能循环利用的物质是 和水。