题目内容
【题目】能源、环境与人类的生活和社会发展密切相关。
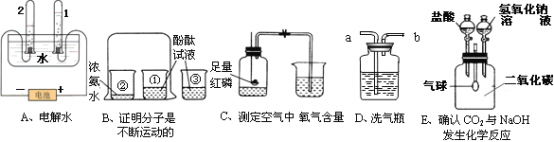
(1)目前,人类以化石燃料为主要能源。煤、石油和______是常见的化石燃料。
(2)下列关于能源与能量的叙述中,正确的是______(填字母序号)。
A.酒精属于可再生能源,适量加入汽油中可作为汽车燃料,减少尾气的污染
B.人类利用的能量都是通过化学反应获得的,最常见的就是燃料的燃烧
C.将煤块粉碎是为了增大与空气的接触面积,使其燃烧充分
D.使化石燃料充分燃烧,不但能节约资源,还能减少对空气的污染
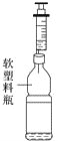
(3)如图所示的甲、乙两个装置(气密性良好),从分液漏斗中加入液体,一段时间后两装置中的气球都胀大(忽略液体体积对气球体积的影响)。精确称量发现:两个实验反应后质量均与反应前数值不相等。

① 两个反应______(填“遵守”或“不遵守”)质量守恒定律。
② 请分别用化学方程式解释两个装置中气球胀大的原因是甲________乙______
【答案】天然气 ACD 遵守 ![]()
![]()
【解析】
(1)目前,人类利用的化石燃料主要包括煤、石油和天然气.
(2)A、酒精用完之后能够再生,属于可再生能源,适量加入汽油中可作为汽车燃料,能够减少尾气的污染,故选项正确;
B、人类利用的能量不都是通过化学反应获得的,例如人类利用的水能、风能、潮汐能等不是通过化学反应获得的,故选项错误;
C、将煤块粉碎是为了增大与空气的接触面积,能够使其燃烧充分,故选项正确;
D、使化石燃料充分燃烧,不但能节约资源,还能减少一氧化碳的排放,从而减少对空气的污染,故选项正确。
(3)①化学反应都遵循质量守恒定律,甲、乙都发生的是化学反应,因此甲、乙两个反应都遵循质量守恒定律;甲中碳酸钠和稀盐酸反应生成氯化钠和二氧化碳,反应方程式为:![]() ,使瓶内压强增大;乙中二氧化碳和澄清石灰水反应生成碳酸钙沉淀和水,反应方程式为:
,使瓶内压强增大;乙中二氧化碳和澄清石灰水反应生成碳酸钙沉淀和水,反应方程式为:![]() ,使瓶内压强减小。
,使瓶内压强减小。

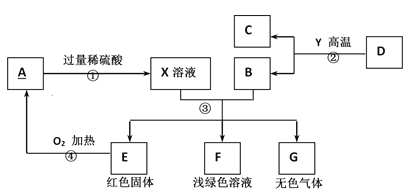
【题目】化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动。
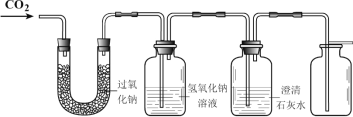
(提供资料)① 二氧化碳与过氧化钠反应生成氧气和另一种物质。② 碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)与盐酸反应均能生成CO2。③ 2Na2O2 + 2H2O === 4NaOH + O2↑。
(1)证明二氧化碳与过氧化钠反应产生氧气并收集一瓶氧气。
同学们在老师的指导下设计了如上图所示装置。
① 如何证明氧气已经收集满______。
② 氢氧化钠溶液的作用是除去未反应的二氧化碳,若观察到______,说明二氧化碳已经除尽。
(2)探究二氧化碳与过氧化钠反应生成的另一种物质。
(猜想与假设)下面是同学们提出的3种猜想。
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
通过对反应物中有关元素的组成分析,你认为猜想______是不正确的,理由是______。
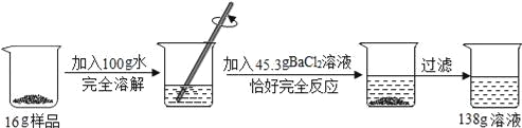
(进行实验)同学们通过以下实验验证了另一种物质,请完成下述实验报告。
实验操作 | 实验现象 | 实验结论 |
取少量CO2与Na2O2反应后的固体于试管中,______。 | 有大量气泡产生,澄清石灰水变浑浊。 | 猜想______是正确的。 |
澄清石灰水变浑浊的化学方程式为______
(反思与评价)若用人呼出的气体通过上图装置,证明二氧化碳与过氧化钠反应生成了氧气,你是否同意这种做法,并阐述理由_______________。