题目内容
【题目】学习了《海水“制碱”》一课后,同学们模拟“侯氏制碱法”进行实验.
(查阅资料)氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
(模拟实验)验证侯氏制碱法能获得纯碱
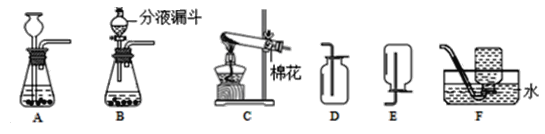
步骤 | 实验装置 | 实验操作及现象 | 解释与结论 |
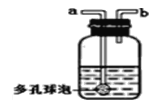
(1) |
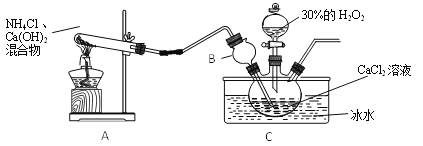
| 先从a管通入____(填 “CO2”或“NH3”),一段时间后,再从b管通入___(填“CO2”或“NH3”),溶液中有固体析出 | 蘸有稀硫酸的棉花可吸收过量的氨气,以免挥发到空气中。 |
(2) |
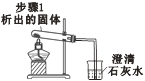
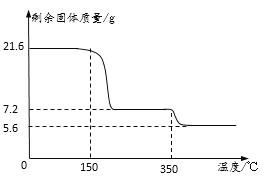
| 充分加热,观察到的现象是:试管口有水珠,烧杯中的导管口有气泡冒出,____。 | 步骤1析出的固体是碳酸氢钠 |
(3) |
| 滴加足量稀盐酸,有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
步骤1发生反应的化学方程式为 ______________。
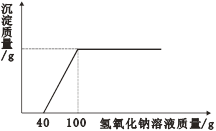
(实验反思)(1)同学们认为步骤3的实验还不足以得出“步骤2加热后得到的固体是纯碱”的结论,经过讨论,大家一致认为需要补充的实验是____________。
(2)也有同学认为制得的纯碱中可能含有氯化钠杂质, 于是又设计了以下实验并得出结论:
实验操作 | 实验现象 | 实验结论 |
_________ | ____________ | 制得的纯碱中含有氯化钠 |
【答案】 NH3 CO2 澄清石灰水变浑浊 NaCl + H2O + NH3 + CO2 = NaHCO3 + NH4Cl 先加入过量氯化钙,观察是否浑浊,取澄清溶液,再滴加盐酸观察是否有气泡。 取纯碱样品于试管中加水溶解,加入过量稀硝酸,后滴几滴硝酸银溶液 先有气泡产生,后产生白色沉淀。
【解析】【模拟实验】(1)氨气极易溶于水,所以a试管应该添加氨气,b试管添加二氧化碳,反之二氧化碳无法充分溶解和反应。
(2)因为碳酸氢钠受热分解生成二氧化碳气体,所以根据结论反推,可以得到二氧化碳使石灰水变浑浊的现象
故可以猜测反应产物为碳酸氢钠,根据元素守恒可得另一物质可能为氯化铵
【实验反思】(1)因为固体还有可能是碳酸氢钠和碳酸钠的混合物。故需要检测其中时候还有碳酸氢钠。所以先加入过量氯化钙,观察是否浑浊,取澄清溶液,再滴加盐酸观察是否有气泡。
(2)要检验氯离子需要用硝酸酸化的硝酸银,硝酸是去除碳酸根的影响,银离子检验氯离子。故现象是先由硝酸和碳酸钠产生气体,然后氯离子和银离子产生沉淀

【题目】化学兴趣小组的同学一起探究金属的化学性质。
(进行实验)
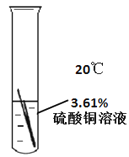
把打磨后的铁丝放入硫酸铜溶液中,铁丝表面有红色固体析出,得出结论:铁和铜的金属活动性顺序是___________。请写出铁丝放入硫酸铜溶液中的反应方程式____________。
(提出问题)
小组同学验证本实验时出现了异常现象:有的试管中铁丝表面没有红色固体出现,反而出现了黑色固体。为了探究此现象,小组同学进行了以下实验:
实验序号 | ① | ② | ③ |
实验 |
|
|
|
观察时间(分钟) | 3 | 3 | 3 |
生成固体颜色 | 黑色 | 红色 | 红色 |
(解释与结论)
(1)通过上述实验能得出铁丝表面有黑色固体产生,与温度有关的实验序号是_________。
(2)通过上述实验除了能得出铁丝表面有黑色固体产生与温度有关,还能得出与_________有关。
(反思与评价)
针对此异常现象,你还想探究的问题是_________。