题目内容
【题目】通过一年的化学学习,你已经掌握了一些实验室制取气体的相关规律,以下是老师提供给大家的一些装置,请你回答下列问题:
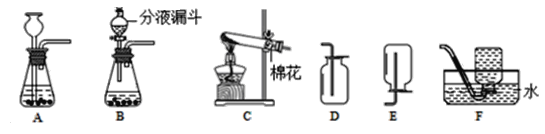
(1)实验室用二氧化锰和过氧化氢溶液制取氧气的化学方程式是________________,若要较好地控制产生氧气的速度,应选用的发生装置是__________(填字母编号)。
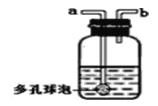
(2)实验室用大理石与稀盐酸制备CO2的化学方程式为_____________, 收集装置最好选择_______(填字母编号)。为了收集干燥的二氧化碳气体,可把气体通过下图的装置中进行干燥再收集。则下图瓶中的溶液是____________(写名称),装置中的多孔球泡的作用是____________。
【答案】 2H2O2 ![]() 2H2O + O2 ↑ B CaCO3+2HCl=CaCl2+2H2O+CO2↑ D 浓硫酸 增大反应物的接触面积
2H2O + O2 ↑ B CaCO3+2HCl=CaCl2+2H2O+CO2↑ D 浓硫酸 增大反应物的接触面积
【解析】本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)实验室用二氧化锰和过氧化氢溶液制取氧气同时生成水,该反应的化学方程式是2H2O2 ![]() 2H2O + O2 ↑;分液漏斗能控制液体的滴加速度,能控制反应的速度。要较好地控制产生氧气的速度,应选用的发生装置是B;
2H2O + O2 ↑;分液漏斗能控制液体的滴加速度,能控制反应的速度。要较好地控制产生氧气的速度,应选用的发生装置是B;
(2)实验室用大理石与稀盐酸制备CO2同时生成氯化钙和水,化学方程式为 CaCO3+2HCl=CaCl2+2H2O+CO2↑,二氧化碳的密度大于空气,能溶于水,一般用向上排空气法收集,收集装置最好选择D,浓硫酸具有吸水性。为了收集干燥的二氧化碳气体,可把气体通过盛有浓硫酸装置中的进行干燥再收集。装置中的多孔球泡能增大反应物的接触面积,使吸收更充分。

 名校课堂系列答案
名校课堂系列答案【题目】某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2(Na2SO3+H2SO4(浓)==Na2SO4+SO2↑+H2O]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(提出问题)①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
(查阅资料)
(1) Na2SO3有较强还原性,在空气中易被氧气氧化:2 Na2SO3+O2==2Na2SO4;
(2) Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(作出猜想)
猜想1:没有变质,成分是Na2SO3;
猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3:_____________________。
(实验探究I)甲、乙两组分别进行实验探究溶液是否变质:
小组 | 实验操作 | 现象 | 结论 |
甲组 | 取少量样品于试管中加入过量稀盐酸; | 产生气泡 | 没有变质,还是Na2SO3 |
乙组 | 取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸。 | _____ | 已部分变质 |
(评价)有同学质疑甲组方案不合理,理由是___________。
(实验探究II)
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略不计)
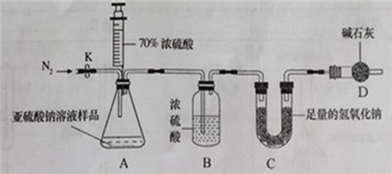
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g。
由此,计算出该溶液中Na2SO3的质量分数为_____________;
(解释)若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的____(填”偏小”或”偏大”)。
乙组仍使用第一次实验的原理,进行如下实验测定Na2SO3溶液的溶质质量分数。
第一步:称取试样ag;
第二步:在溶液中加入过量氯化钡溶液和足量稀盐酸;
第三步:过滤、洗涤、烘干沉淀;
第四步:称量沉淀的质量为bg;
第五步:计算溶液中Na2SO3的溶质质量分数=(1-142b/233a)×100%。
试完成下列问题:
(1)加入氯化钡溶液过量的目的是________________;
(2)第三步操作要洗涤沉淀的原因是______________________;
(反思)由此可得出,保存亚硫酸钠时应___________________________。
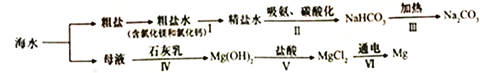
【题目】学习了《海水“制碱”》一课后,同学们模拟“侯氏制碱法”进行实验.
(查阅资料)氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
(模拟实验)验证侯氏制碱法能获得纯碱
步骤 | 实验装置 | 实验操作及现象 | 解释与结论 |
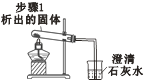
(1) |
| 先从a管通入____(填 “CO2”或“NH3”),一段时间后,再从b管通入___(填“CO2”或“NH3”),溶液中有固体析出 | 蘸有稀硫酸的棉花可吸收过量的氨气,以免挥发到空气中。 |
(2) |
| 充分加热,观察到的现象是:试管口有水珠,烧杯中的导管口有气泡冒出,____。 | 步骤1析出的固体是碳酸氢钠 |
(3) |
| 滴加足量稀盐酸,有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
步骤1发生反应的化学方程式为 ______________。
(实验反思)(1)同学们认为步骤3的实验还不足以得出“步骤2加热后得到的固体是纯碱”的结论,经过讨论,大家一致认为需要补充的实验是____________。
(2)也有同学认为制得的纯碱中可能含有氯化钠杂质, 于是又设计了以下实验并得出结论:
实验操作 | 实验现象 | 实验结论 |
_________ | ____________ | 制得的纯碱中含有氯化钠 |
【题目】下列选项中相关量的变化与图像不相符的是
选项 | X | Y |
|
A.向一定量饱和食盐水中加水 | 水的质量 | 溶质质量 | |
B.向一定量锌粒中加稀硫酸 | 稀硫酸质量 | 氢气质量 | |
C.向一定量CuCl2溶液中加NaOH溶液 | NaOH溶液质量 | 沉淀质量 | |
D.向一定量水中加KNO3晶体 | KNO3晶体质量 | 溶质质量分数 | |
A. A B. B C. C D. D