题目内容
有一研究性学习小组为测定某铜锌合金的成分,取10g该合金经粉碎后放入烧杯中,再加入足量的稀硫酸,反应过程中烧杯内固体物质的质量与反应时间的关系如下图所示。请回答下列问题。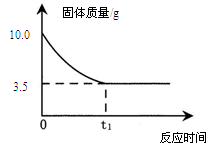
(1)将合金粉碎的目的是 。
(2)10g合金中铜的质量为 g。
(3)充分反应后产生的氢气质量为多少?
(1).能使反应充分进行 (2)3.5 (3)0.2
解析试题分析:(1)将合金粉碎后,增大合金与硫酸硫酸反应的面积,可使二者的反应更剧烈和充分。
(2)在铜锌合金中,铜与稀硫酸不反应,锌可与稀硫酸反应。从图中可知不能反应的固体的质量为3.5 g,即合金中铜的质量。
(3)解题思路:锌可与稀硫酸反应生成氢气。可先出锌的质量,再根据锌与氢气在反应中的质量关系求出氢气的质量。解题过程如下:
解:合金中锌的质量为:10g —3.5 g=" 6.5g"
设生成氢气的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
6.5g x
65:2 =6.5g:x
x=0.2g
答:生成氢气的质量为0.2g。
考点:金属活动性顺序、根据化学方程式的计算

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目