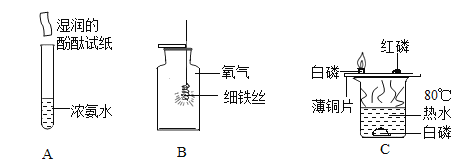
题目内容
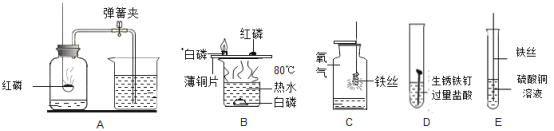
【题目】小芳设计了如下气体制取与性质验证的组合装置。打开分液漏斗活塞放出一定量过氧化氢溶液后,关上活塞,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题。
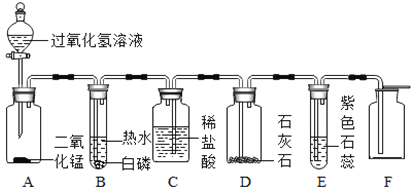
(1)B中白磷能够在水下燃烧的原因是________。
(2)D中发生反应的化学方程式为________。
(3)E中的实验现象是________。
(4)用F装置收集气体的依据是_______。
【答案】A中生成的O2进入B中,热水中的白磷达到着火点,同时与O2接触 ![]() 紫色石蕊试液变红 CO2的密度大于空气的密度
紫色石蕊试液变红 CO2的密度大于空气的密度
【解析】
(1)过氧化氢分解生成的氧气进入B中,提供了燃烧所需要的氧气,B中的白磷达到着火点,同时与O2接触,因此B中白磷能够在水下燃烧;
(2)A中生成的氧气使装置内的压强增大,能将盐酸压入D中,使盐酸与碳酸钙反应生成氯化钙、水和二氧化碳气体,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)二氧化碳进入E中,二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊试液变红;
(4)F是向上排空气法收集气体,能使用此法收集的气体需要具备密度比空气大的性质。

【题目】化学兴趣小组在实验室发现一瓶氢氧化钠溶液,瓶口有少量白色固体且玻璃瓶塞打不开,这一情况激起了他们浓厚的兴趣,于是展开了如下探究:
(提出问题)
瓶口白色固体的成分是什么?
(查找资料)
(1)玻璃中含有二氧化硅(SiO2),试剂瓶身经抛光处理,不易反应,而瓶口和玻璃塞上的磨砂将二氧化硅裸露出来。
(2)二氧化硅能与氢氧化钠溶液反应,![]()
(3)硅酸钠(Na2SiO3)是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性;硅酸钠溶液能与强酸反应,如:![]() (白色);硅酸钠溶液能与氯化钙溶液反应:
(白色);硅酸钠溶液能与氯化钙溶液反应:![]() (白色)。
(白色)。
(作出猜想)
白色固体的成分是:1.硅酸钠:Ⅱ,硅酸钠和碳酸钠:Ⅲ硅酸钠、碳酸钠和氢氧化钠
(实验探究)
取一定量白色固体溶于适量水中形成样品溶液,分组进行如下实验并相互评价:
实验操作 | 实验现象 | 结论与评价 | ||
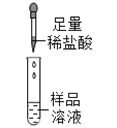
第 一 组 |
| 有气泡冒出且产生白色沉淀 | 同学们认为猜想____不成立 | |
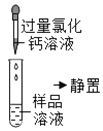
第 二 组 | 第 一 步 |
| 产生白色沉淀 | 第一组的同学认为:此步骤还不能准确判断出原固体的成分。原因是________ |
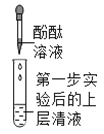
第 二 步 |
| _______ | 大家一致认为: 猜想Ⅱ成立 | |
(解释结论)
猜想Ⅱ中碳酸钠的来源是________(用化学方程式表示)。
(反思交流)
(1)有同学认为,第二组实验中不能用氢氧化钙溶液代替氯化钙溶液,理由_______;
(2)氢氧化钠溶液必须密封保存,且试剂瓶只能用橡胶塞或软木塞。