题目内容
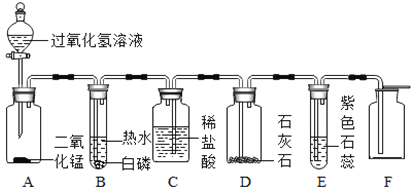
【题目】如图是实验室用于气体制备的装置,请根据图示回答问题:
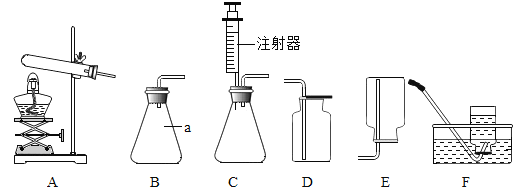
(1)图中a装置的名称是______。
(2)实验室中能用于过氧化氢溶液制氧气,且便于随时添加液体药品的发生装置是______(填序号,下同);要想得到比较纯净的氧气,需要选择的收集装置是______。
(3)实验室制取二氧化碳时,应选择的收集装置是______,理由是______;判断二氧化碳是否收集满的方法是______,制备二氧化碳气体的方程式为______。
【答案】锥形瓶 C F D CO2密度大于空气且能溶于水 将燃着木条放在集气瓶口,熄灭则满 CaCO3+2HCl=CaCl2+CO2↑+H2O
【解析】
(1)锥形瓶是常用的反应容器,a装置的名称是:锥形瓶。
(2)注射器便于随时添加液体药品,选择发生装置是C。氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净,选择的收集装置是F。
(3)二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,收集装置是D。二氧化碳的验满方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了。制备二氧化碳气体的方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;

【题目】以下是某研究小组探究影响化学反应速率快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
① | 5 | 12 | 20 | 0.2 | 125 | 11 |
② | 30 | 12 | 20 | 0.2 | 125 | 2 |
③ | 30 | 12 | 40 | / | 125 | 148 |
④ | 30 | 12 | 90 | / | 125 | 82 |
(1)通过实验①和②对比可知,化学反应快慢与_____有关;
(2)通过对比实验_____和_____可知(填序号),化学反应快慢与温度的关系是_____。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是_____。
(4)写出该反应的化学方程式_____。