题目内容
【题目】在学习《制取氧气》时,小明突发奇想:除了书上介绍的三种原理,是否可以用其他药品来制得氧气呢?对此,他带领学习小组进行了以下探究。
针对小明的突发奇想,这属于科学探究的_____环节。小组同学求助老师得知,可以用一些过氧化物如过氧化钠、过氧化钙等进行试验。
〖提出问题〗过氧化钙可否用于制取氧气。
〖查阅资料〗部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,同时得到氧化钙。当与水接触时,也能生成氧气,同时得氢氧化钙。可做鱼池增氧剂、泳池杀菌剂等。
〖猜想与验证〗
(1)猜想Ⅰ:加热过氧化钙可制取氧气。
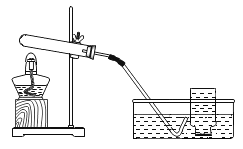
实验装置 | 实验主要过程 |
| ①检验装置的气密性。操作如下:先将导管一段伸入液面以下,用手紧握试管,观察到_____,松手后,_____。 ②加入过氧化钙,加热,试管口略向下倾斜的原因是_____,导管口有大量的气泡冒出。 ③收集满一瓶气体。验满的方法是_____。 ④停止加热。熄灭酒精灯前,应先_____。 ⑤检验气体。方法是_____。 |
实验结论:加热过氧化钙可制取氧气。反应的文字表达式为_____,基本反应类型为_____。
(2)猜想Ⅱ:过氧化钙与水反应可迅速制取大量氧气。
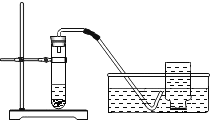
实验装置 | 实验主要过程 |
| ①检验装置的气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后,仍有少量的细小气泡缓慢放出。收集并检验所得气体,确为氧气。 |
实验结论:不能用过氧化钙与水反应迅速制取大量氧气。
分析与反思:
①虽然没有快速收集到大量氧气,但渔民用过氧化钙做增氧剂的原因是_____。
②学习小组希望对此实验进行改进,使该反应加快。你的合理的建议是_____。
【答案】提出问题 导管口有气泡冒出 导管内形成一段液柱 防止水倒流使试管炸裂 将带火星的木条放在集气瓶口,木条复燃,证明已集满氧气 先将导管移出水面 将带火星的木条伸入集气瓶内,木条复燃证明气体是氧气 :过氧化钙![]() 氧化钙+氧气 分解反应 过氧化钙和水可以缓慢反应,释放出氧气 将过氧化钙粉碎(或其他合理答案)。
氧化钙+氧气 分解反应 过氧化钙和水可以缓慢反应,释放出氧气 将过氧化钙粉碎(或其他合理答案)。
【解析】
在学习《制取氧气》时,小明突发奇想:除了书上介绍的三种原理,是否可以用其他药品来制得氧气呢? 小明的突发奇想,这属于科学探究的提出问题环节;
[猜想与验证]
(1)猜想Ⅰ:①检验装置的气密性。操作如下:先将导管一端伸入液面以下,用手紧握试管,此时,试管内的气体受热膨胀,压强增大,从导管口逸出,观察到导管口产生气泡,松手后,温度降低,气体减少,水进入导管内,形成一段液柱;
②由于药品在放置时接触到空气,所以药品不会绝对干燥,总有一定的水分。加热时,水蒸气逸出,在试管口处冷凝成液体,加热过氧化钙时,试管口略向下倾斜的原因是防止水倒流使试管炸裂;
③过氧化钙在加热条件下分解生成氧气,收集满一瓶气体。验满的方法是将带火星的木条放在集气瓶口,木条复燃,证明已集满氧气;
④熄灭酒精灯前,应先将导管移出水面,否则易导致水倒流入试管内,使试管骤冷而炸裂;
⑤检验氧气的方法是将带火星的木条伸入集气瓶内,木条复燃,证明气体是氧气;
由题干中信息可知,过氧化钙(CaO2)室温下稳定,在受热时分解生成氧气,同时得到氧化钙。反应的文字表达式为:过氧化钙![]() 氧化钙+氧气;基本反应类型为分解反应;
氧化钙+氧气;基本反应类型为分解反应;
(2)猜想Ⅱ:①虽然没有快速收集到大量氧气,但过氧化钙和水可以缓慢反应,释放出氧气,增大水中氧气的溶解的量;
②学习小组希望对此实验进行改进,使该反应加快。合理的建议是将过氧化钙粉碎,增大过氧化钙和水的接触面积,提高反应速率(或气体合理答案)。

 阅读快车系列答案
阅读快车系列答案