题目内容
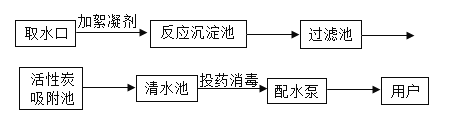
【题目】某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2。小青同学设计了以下实验方案来除去可溶性杂质。
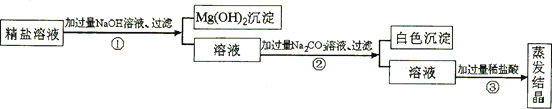
(1)步骤①的化学方程式为___________。
(2)步骤②中得到的白色沉淀是_________(填化学式)。
(3)步骤③中加稀盐酸是为了除去溶液中的______。
A CaCl2 B MgCl2 C NaOH D Na2CO3
【答案】2NaOH+MgCl2=2NaCl+Mg(OH)2↓ CaCO3 CD
【解析】
除钙离子用碳酸根离子,除镁离子用氢氧根离子,加入的试剂都是过量的,后加的试剂要把先加的试剂所带入的杂质除掉,加入过量的稀盐酸,这样可以除去多余的碳酸根离子和氢氧根离子
(1)步骤①的反应是氢氧化钠和氯化镁生成氢氧化镁和氯化钠,反应的化学方程式为2NaOH+MgCl2=2NaCl+Mg(OH)2↓。
(2)步骤②反应是碳酸钠和氯化钙生成碳酸钙和氯化钠,得到的白色沉淀是碳酸钙,化学式为CaCO3。
(3) 加适量盐酸,与①中过量NaOH溶液和②中过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体;蒸发、结晶,得到精盐,步骤③中加稀盐酸是为了除去溶液中的氢氧化钠和碳酸钠,故选CD。

 名校课堂系列答案
名校课堂系列答案【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2 杂质。用该矿石制备 Mg(OH)2 的工艺流程简图如图:
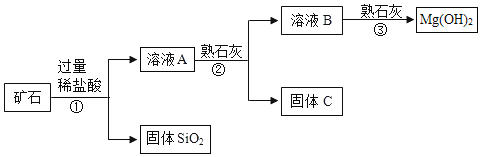
回答下列问题:
(1)步骤①和步骤②均用到的操作是_____________;
(2)步骤①中加过量稀盐酸的目的是______________;
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为________________。
【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
查阅资料
a.固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。
b.氯化钙、氯化溶液均呈中性。
(提出问题)
①酒精中是否含有碳元素?
②固体酒精中的氢氧化钠是否变质?
(实验探究)
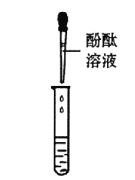
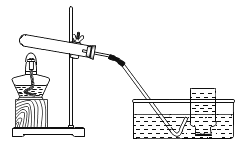
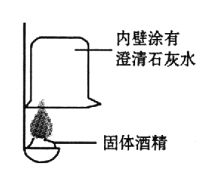
①按右图所示进行实验,发现烧杯内壁有一层白膜,可得出酒精中含有碳元素的结论,理由是_______________。
②取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的:_______________由此说明氢氧化钠已变质。
③为进一步确定氢氧化钠的变质程度,分组进行探究。
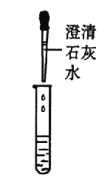
甲组同学取烧杯上层清液于两支试管中,按下图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生______________ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是_______________
他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)乙组实验中加足量氯化钡溶液的目的是_____________
(实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。
【题目】在学习《制取氧气》时,小明突发奇想:除了书上介绍的三种原理,是否可以用其他药品来制得氧气呢?对此,他带领学习小组进行了以下探究。
针对小明的突发奇想,这属于科学探究的_____环节。小组同学求助老师得知,可以用一些过氧化物如过氧化钠、过氧化钙等进行试验。
〖提出问题〗过氧化钙可否用于制取氧气。
〖查阅资料〗部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,同时得到氧化钙。当与水接触时,也能生成氧气,同时得氢氧化钙。可做鱼池增氧剂、泳池杀菌剂等。
〖猜想与验证〗
(1)猜想Ⅰ:加热过氧化钙可制取氧气。
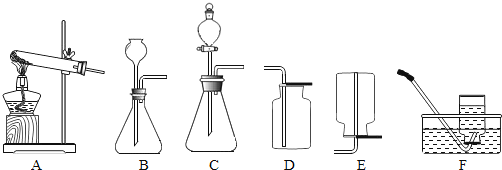
实验装置 | 实验主要过程 |
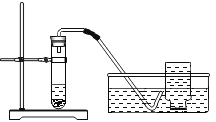
| ①检验装置的气密性。操作如下:先将导管一段伸入液面以下,用手紧握试管,观察到_____,松手后,_____。 ②加入过氧化钙,加热,试管口略向下倾斜的原因是_____,导管口有大量的气泡冒出。 ③收集满一瓶气体。验满的方法是_____。 ④停止加热。熄灭酒精灯前,应先_____。 ⑤检验气体。方法是_____。 |
实验结论:加热过氧化钙可制取氧气。反应的文字表达式为_____,基本反应类型为_____。
(2)猜想Ⅱ:过氧化钙与水反应可迅速制取大量氧气。
实验装置 | 实验主要过程 |
| ①检验装置的气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后,仍有少量的细小气泡缓慢放出。收集并检验所得气体,确为氧气。 |
实验结论:不能用过氧化钙与水反应迅速制取大量氧气。
分析与反思:
①虽然没有快速收集到大量氧气,但渔民用过氧化钙做增氧剂的原因是_____。
②学习小组希望对此实验进行改进,使该反应加快。你的合理的建议是_____。