题目内容
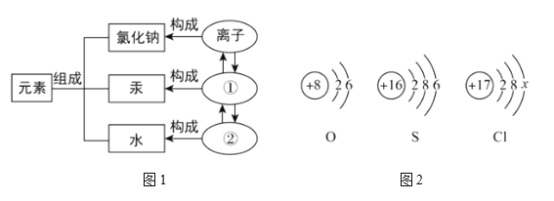
【题目】四硫化钠(Na2S4)固体可代替红磷测定空气中氧气的体积分数,反应原理为:
2Na2S4 + O2 + 2H2O = 8S↓ + 4NaOH
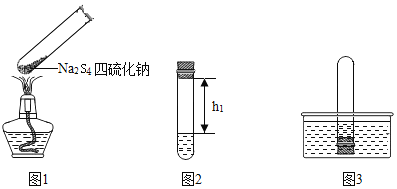
(实验资料)①上述反应过程中温度变化不明显。
②Na2S4、NaOH均可溶于水。S为淡黄色粉末,不溶于水。
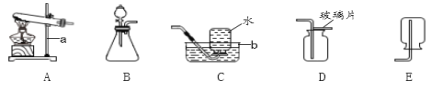
(实验过程)①取适量四硫化钠固体放于试管中(如图1所示,夹持装置已略去)
②向该试管中加入10ml水,迅速塞进橡皮塞,充分震荡,测量液面至橡胶塞下沿的距离,记录数据 h1(如图2所示)。
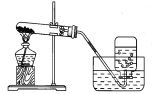
③将该试管插入水中(如图3所示)。拔下橡皮塞,观察到____________ 。塞紧橡皮塞,将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据 h2,理论上h1 :h2 =___________ 。
④按照①-③再重复实验2次,3次实验数据如下表所示。
第1次 | 第2次 | 第3次 | |
h1/cm | 11.0 | 11.4 | 11.6 |
h2/cm | 8.7 | 9.1 | 9.2 |
(解释与结论)根据第2次实验数据,计算空气中氧气的体积分数为___________%(结果精确到0.1%)
(反思与评价)在实验过程中,若向试管中加水后没有迅速塞紧橡皮塞,则所测定的空气中氧气的体积分数将会____________(填“偏大”、“偏小”或“无影响”).
【答案】水进入试管内,进入水的体积约为试管内空气体积的五分之一,有黄色固体生成;5:4;20.2%;偏小
【解析】
实验过程:③将该试管倒插入水中,取下橡皮塞,待试管中液面不再上升后塞紧橡皮塞,将试管取出,倒过来测量液面至橡胶塞下沿的距离为h2,由于氧气约占空气总体积的五分之一,因此h1:h2=h1:(h1-![]() h1)=5:4;
h1)=5:4;
解释与结论:根据第2次实验数据,空气中氧气的体积分数为:![]() ×100%=20.2%;
×100%=20.2%;
反思与评价:在实验过程中,若向试管中加水后没有迅速塞紧橡皮塞,则随着氧气的消耗,装置外的空气不断进入装置中,会导致装置中除氧气外的气体增多,从而导致所测定的空气中氧气的体积分数偏小。