题目内容
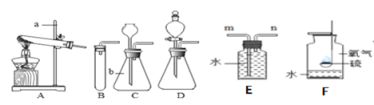
【题目】如图是“空气中氧气体积分数测定”实验的改进装置。主要操作是:在实际容积为180ml的集气瓶里,先装进50ml的水,再按图连接好仪器,按下热的玻璃棒,白磷立即被点燃。(白磷40℃即燃烧,燃烧产物与红磷相同)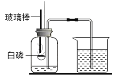
(1)该实验中白磷需稍过量,目的是_____________。
(2)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是________________;若实验成功,最终集气瓶中水的体积约为_____ml。
(3)若将白磷换成木炭,该实验______(能或否)获得成功。原因是:____。
(4)集气瓶里预先装进的50ml水,在实验过程中起到的作用是____________________。
A、加快集气瓶内气体冷却 B、液封导气管末端以防气体逸出 C、吸收五氧化二磷
【答案】充分消耗集气瓶内的氧气先下降后上升76否木炭燃烧虽然能消耗氧气,但会生成新的气体,不会使瓶内气压明显降低ABC
【解析】
(1)白磷过量能够将集气瓶中的氧气尽可能的消耗掉,使实验结果更准确;
(2)白磷燃烧放出热量,所以开始燃烧到结束实验,集气瓶中的气体受热膨胀而使集气瓶中液体进入烧杯中,然后集气瓶冷却后,氧气被消耗而使集气瓶中压强减小,从而使烧杯中的水进入集气瓶中,所以是先下降后上升;集气瓶的容积为180mL,在加入50mL水后剩余的容积为130mL,而氧气约占空气体积的五分之一,所以反应完全并冷却后进入集气瓶的水的体积为26mL,故最终集气瓶中水的体积为:50mL+26mL=76mL;
(3)炭粉和氧气反应生成了二氧化碳,不能产生集气瓶内外的压强差,所以实验不能成功;
(4)在集气瓶里预先装进的50mL水,在实验过程中可以加快集气瓶冷却、液封导气管末端以防气体逸出并且能够缓冲集气瓶内气压的骤然升高。故选ABC。

 阅读快车系列答案
阅读快车系列答案【题目】四硫化钠(Na2S4)固体可代替红磷测定空气中氧气的体积分数,反应原理为:
2Na2S4 + O2 + 2H2O = 8S↓ + 4NaOH
(实验资料)①上述反应过程中温度变化不明显。
②Na2S4、NaOH均可溶于水。S为淡黄色粉末,不溶于水。
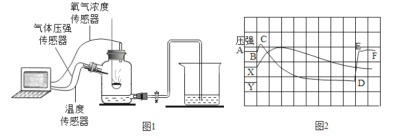
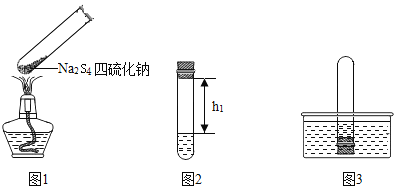
(实验过程)①取适量四硫化钠固体放于试管中(如图1所示,夹持装置已略去)
②向该试管中加入10ml水,迅速塞进橡皮塞,充分震荡,测量液面至橡胶塞下沿的距离,记录数据 h1(如图2所示)。
③将该试管插入水中(如图3所示)。拔下橡皮塞,观察到____________ 。塞紧橡皮塞,将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据 h2,理论上h1 :h2 =___________ 。
④按照①-③再重复实验2次,3次实验数据如下表所示。
第1次 | 第2次 | 第3次 | |
h1/cm | 11.0 | 11.4 | 11.6 |
h2/cm | 8.7 | 9.1 | 9.2 |
(解释与结论)根据第2次实验数据,计算空气中氧气的体积分数为___________%(结果精确到0.1%)
(反思与评价)在实验过程中,若向试管中加水后没有迅速塞紧橡皮塞,则所测定的空气中氧气的体积分数将会____________(填“偏大”、“偏小”或“无影响”).