题目内容
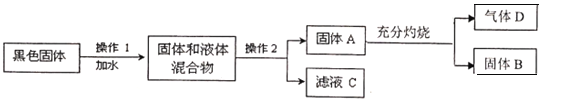
【题目】河水含泥沙、细菌等杂质,需要净化处理成自来水。某市自来水厂的生产过程如下图所示:
![]()
(1)沉淀池中加入明矾的目的是________________________。
(2)沙滤池可将________过滤除去。
(3)要鉴别自来水是软水还是硬水,可向自来水样品中加入适量的________________,搅拌,如果观察到________________,则样品为软水。
(4)下列操作中,能够降低水的硬度的是________(填字母序号)。
A.静置 B.过滤 C.煮沸 D.蒸馏
【答案】吸附水中悬浮颗粒物并使之沉淀;泥沙等不溶性杂质;肥皂水;产生较多泡沫,较少浮渣;CD
【解析】
(1)明矾可溶于水,具有吸附性,故用来作为净水剂;(2)过滤可以将不溶于水的杂质过滤掉;(3)软水加入肥皂水搅拌会有泡沫出现,硬水会产生浮渣,故可以检验软水和硬水;(4)煮沸和蒸馏使水气化、液化,可以得到纯净的水,去除杂质元素,故可以得到硬度低的水,故选CD。

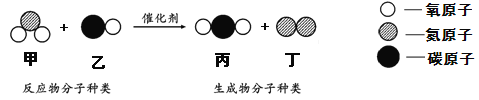
【题目】学习了二氧化锰对过氧化氢有催化作用的知识后。某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行了如下探究。
(猜想)Ⅰ.氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ.氧化铜是反应的催化剂,反应前后_____和_____不变。
(实验)用天平称量0.2g氧化铜,取5mL 5%的过氧化氢溶液于试管中,进行如下实验:
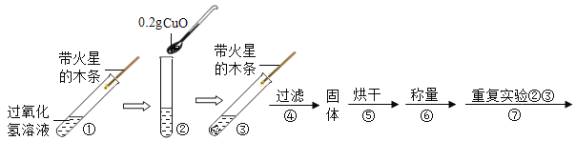
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____, 带火星的木条复燃 | 所得固体 _____g | 溶液中有气泡放出, _____ | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(2)步骤①的目的是_____。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为_____。
【题目】四硫化钠(Na2S4)固体可代替红磷测定空气中氧气的体积分数,反应原理为:
2Na2S4 + O2 + 2H2O = 8S↓ + 4NaOH
(实验资料)①上述反应过程中温度变化不明显。
②Na2S4、NaOH均可溶于水。S为淡黄色粉末,不溶于水。
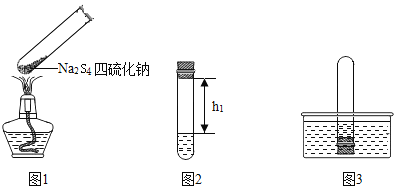
(实验过程)①取适量四硫化钠固体放于试管中(如图1所示,夹持装置已略去)
②向该试管中加入10ml水,迅速塞进橡皮塞,充分震荡,测量液面至橡胶塞下沿的距离,记录数据 h1(如图2所示)。
③将该试管插入水中(如图3所示)。拔下橡皮塞,观察到____________ 。塞紧橡皮塞,将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据 h2,理论上h1 :h2 =___________ 。
④按照①-③再重复实验2次,3次实验数据如下表所示。
第1次 | 第2次 | 第3次 | |
h1/cm | 11.0 | 11.4 | 11.6 |
h2/cm | 8.7 | 9.1 | 9.2 |
(解释与结论)根据第2次实验数据,计算空气中氧气的体积分数为___________%(结果精确到0.1%)
(反思与评价)在实验过程中,若向试管中加水后没有迅速塞紧橡皮塞,则所测定的空气中氧气的体积分数将会____________(填“偏大”、“偏小”或“无影响”).