题目内容
【题目】实验是实现科学探究的重要途径,请回答下列有关化学实验的问题。
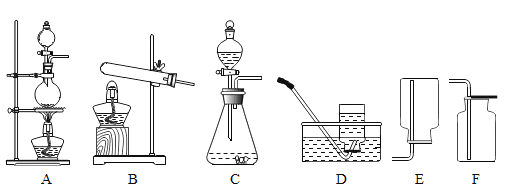
(1)利用B装置制取种气体,写出有关反应的化学方程式。___________________
(2)实验室可用氯化钠固体和浓硫酸在加热条件下反应制取氯化氢气体,该气体极易溶于水,则制取氯化氢应选择的发生装置和收集装置分别为______________ (填字母)。
【答案】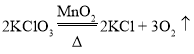 AF
AF
【解析】
(1)利用B装置制取气体,由于试管口没有塞一团棉花,应该是利用氯酸钾和二氧化锰制取,反应的化学方程式: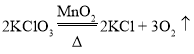 ;
;
(2)实验室用氯化钠固体和浓硫酸在加热条件下反应制取氯化氢气体,应该用A装置作为发生装置;该气体极易溶于水,不能用排水法收集,氯化氢气体密度比空气大,可以用向上排空气法收集,即用F装置收集;

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
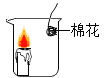
金牌教辅培优优选卷期末冲刺100分系列答案【题目】新年联欢晚会上,老师给同学们表演了一个魔术:大烧杯中盛有一只燃着的蜡烛和一团包有过氧化钠(Na2O2)的棉花,将一瓶二氧化碳倒入烧杯中,蜡烛慢慢的熄灭,然后棉花突然剧烈的燃烧起来。这出乎意料的现象引起了同学们的极大兴趣,请你参与同学们的讨论和探究。
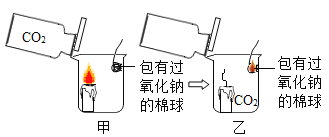
蜡烛熄灭的原因是_______________。
(提出问题)棉花为什么会燃烧?
(提出猜想)
(1)可能是蜡烛燃烧引燃了棉花。
(2)可能是二氧化碳与过氧化钠反应生成了氧气。
(3)_____________。
(实验验证)
序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
① | 按下图所示装置进行实验
| 无现象 | 猜想(1)____________(填“成立”或“不成立”) |
② | 向盛满二氧化碳的集气瓶中加入适量的过氧化钠粉末,充分振荡,并______________ | ________ | 二氧化碳与过氧化钠反应生成了氧气,猜想(2)成立 |
③ | _____________ | ______ | 猜想(3)成立 |
(实验结论)
(1)CO2与Na2O2反应生成了氧气与一种化合物,化学方程式为______________。
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。
【题目】化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究。
(提出问题)这是一瓶什么溶液?
(猜想与假设)海天同学的猜想是Na2SO3溶液;刘浩同学的猜想是Na2SO4溶液;你的猜想是_____(写一种)。
(查阅资料)
Ⅰ.白色沉淀BaSO3不溶于水,但要溶于稀盐酸。
Ⅱ.硝酸具有强氧化性,能将BaSO3氧化成BaSO4。
Ⅲ.Na2SO3与稀盐酸反应产生SO2,SO2能使石灰水变浑浊,也能使品红溶液褪色。
(进行实验)
Ⅰ.海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想成立,而刘浩同学认为他的结论不合理,原因是_____。
Ⅱ.刘浩同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为_____,刘浩同学认为自己的猜想成立。
Ⅲ.卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl2和稀硝酸,Na2SO3也会产生沉淀,为了验证自己的观点,做了如下实验:
步骤 | 操作 | 实验现象 | 实验结论 |
步骤1 | 取少量该溶液于试管中,滴加足量的BaCl2溶液 | _______ | 无 |
步骤2 | 向步骤1的试管中滴加足量的稀盐酸 | _______ | 此溶液不是Na2SO4 |
步骤3 | 将步骤2中产生的气体通入品红溶液 | 品红溶液褪色 | _______ |
写出卓玛同学实验过程中的化学方程式:___________,__________。
【题目】某校化学兴趣小组在探究“酸碱盐的相关性质”时,做了如图一所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图所示),观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。
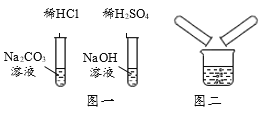
(查阅资料)Na2SO4溶液、NaCl溶液呈中性。
(提出猜想)猜想1:Na2SO4、NaCl;
猜想2:Na2SO4、NaCl和_____;
猜想3:Na2SO4、NaCl和H2SO4;
猜想4:Na2SO4、NaCl、H2SO4和Na2CO3。
(交流讨论)小强同学认为猜想4一定是错误的,他的理由是_____(用化学方程式表示)。
(进行实验)小明同学设计如下两个实验方案:
实验步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液 | _____ | 猜想3正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中,加入少量铁粉 | _____ |
请写出方案二中有关反应的化学方程式:_____。
(反思与总结)分析反应后溶液中溶质成分,除要考虑生成物外,还需考虑反应物是否过量。