题目内容
【题目】2018.4月国家药监部门查处了一批利用废旧皮革加工药用胶囊的不法厂家。这种方法生产的胶囊重金属元素铬严重超标,对人民群众的身心健康造成极大危害。右图是铬元素的部分信息,下列有关说法正确的是

A. 一个铬原子中含24个质子 B. 铬的相对原子质量是24
C. 铬属于非金属元素 D. 化学科学对人类来说是过大于功
【答案】A
【解析】A、从元素周期表中铬元素的信息可知,铬的原子序数是24,依据质子数等于原子序数,所以一个铬原子中含24个质子,正确;B、从元素周期表中铬元素的信息可知,铬的相对原子质量是52.00,错误;C、铬元素带“钅”字旁,属于金属元素,错误; D、化学在保证人类的生存并不断提高人类的生活质量方面起着非常重要的作用,所以化学对人类来说是功大于过,错误。故选A。

 考前必练系列答案
考前必练系列答案【题目】某兴趣小组在制取氧气的实验过程中,有同学联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,于是做出猜想:过氧化钙与水反应可制取氧气。
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应_____(填“能”或“不能”)用于实验室制取氧气。
【分析与反思】
(1)小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议_____。
(2)同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气。你认为猜想_____(填序号)一定是错误的,理由是_____
【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
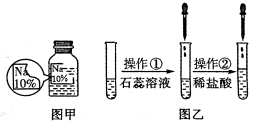
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。