题目内容
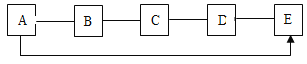
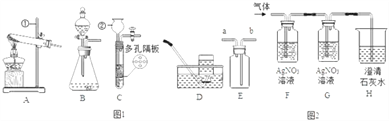
【题目】素有“铜都”之称的安徽铜陵有许多黄铜矿(主要成分为CuFeS2)。黄铜矿经初步 处理后,所得溶液甲中的溶质为 Fe2(SO4)3、CuSO4及H2SO4。某同学通过废铁屑与溶液甲反 应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示:
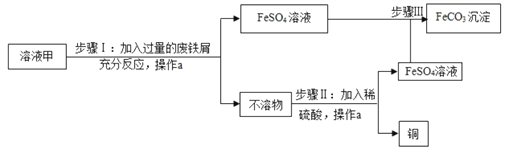
(1)Fe2(SO4)3与铁反应的化学方程式如下,请配平:xFe2(SO4)3+yFe=zFeSO4,其中x、y、z为化学计量数,z的值为_____;
(2)步骤Ⅰ中,生成铜的化学方程式:_________。废铁屑含有少量铁锈,对产物的成分没有影响,原因是_____;
(3)操作a名称为_____,为提高操作a的速率,可以采取的方法有_____;
(4)不溶物的成分为_____ (填化学式)。
【答案】 3 Fe+CuSO4=Cu+FeSO4 氧化铁和硫酸反应生成的硫酸铁再和铁反应生成 硫酸亚铁 过滤 先静置,再过滤 Cu、Fe(全对得分)
【解析】本题考查了金属的性质,过滤,化学方程式的配平等。首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答。
(1)将方程式xFe2(SO4)3+yFe=zFeSO4配平得:Fe2(SO4)3+2Fe=3FeSO4,z的值为3;
(2)溶液甲中含有硫酸铜,硫酸铜和加入的铁屑反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是氧化铁和硫酸反应生成的硫酸铁,再和铁反应生成硫酸亚铁;
(3)由流程图可知,操作a是将固体与液体分离,名称是过滤,为提高操作a的速率,可以采取的方法有先静置,再过滤;
(4)所得“不溶物”中含两种金属,其成分是剩余的铁和置换出的铜化学式是Fe、Cu。

【题目】碘被公认为人类的“智慧元素”,如图是元素周期表中关于碘元素的信息。下列关于碘元素的说法错误的是
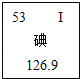
A.碘元素是非金属元素 B.相对原子质量为126.9g
C.原子核内质子数为53 D.原子序数为53
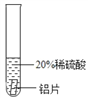
【题目】(题文)小彬同学新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在 学习金属化学性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动。
(查阅资料)
①铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液……
(预测)三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
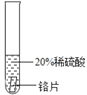
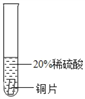
(实验过程)取大小相同的三种金属片,用砂纸打磨光亮。
实验一 | 实验二 | 实验三 | |
实 验 方案 |
|
|
|
实 验现象 | ______________ | ____________ | _______ |
结论 | 铬 与 稀 硫 酸 可 以 反应,速度较慢 | 铜不与稀硫酸反应 | _____ |
三种金属在金属活动性顺序表中的相对位置关系是_____ | |||
(回答问题)
(1)将上表中三处划横线的位置填上适当的内容。
(2)用砂纸打磨金属片的目的是_____。
(3)实验一所发生反应的化学方程式是_____。
(4)小东提出用硫酸铝溶液代替上述实验中的稀硫酸,小燕认为不可行,理由是_____。
(5)上述实验用了四种药品,小清认为只要选用三种药品进行实验就可以得出三种金属在 金属活动性顺序表中的相对位置关系,这三种药品可以是_____。
(6)实验发现,相等浓度的盐酸和硫酸,盐酸和铝反应的速率比硫酸快得多,可能的原因是:_____,请设计实验证明你的猜想____________。