题目内容
【题目】在实验室里,某同学看到氢氧化钠试剂瓶的瓶口有白色粉末,他对白色粉末的成分作出了一些猜测。
猜测一:可能是氧氧化钠 猜测二:可能是碳酸钠 猜测三:可能是氧氧化钠和碳酸钠
为探究白色粉末的成分,他将该粉末溶于水,得到无色溶液,再迸行了如下实验:
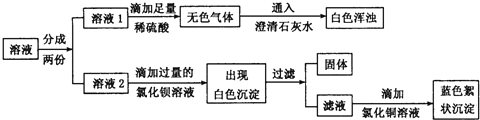
(1)根据实验现象推测,无色气体是________。
(2)在溶液2中滴加过量氯化钡溶液的目的是____________________
(3)由实验现象可知,猜测___是正确的,写出产生蓝色絮状沉淀的化学方程式__________________。
【答案】 CO2 除去碳酸钠,避免干扰实验 三 2 NaOH + CuCl2==Cu(OH)2↓ + 2NaCl
【解析】(1)能使澄清石灰水变浑浊的气体是二氧化碳。(2)在溶液2中滴加过量氯化钡溶液的目的是除去碳酸钠,避免干扰氢氧化钠的检验。(3)取溶液,滴加稀硫酸,有气体生成,将生成的气体通入澄清石灰水中,澄清石灰水变浑浊,说明溶液中含有碳酸钠。另取溶液,滴加过量的氯化钡溶液,产生白色沉淀,过滤,向滤液中滴加氯化铜溶液,产生蓝色絮状沉淀,说明溶液中含有氢氧化钠,所以猜想三成立,产生蓝色絮状沉淀的化学方程式:2NaOH+CuCl2==Cu(OH)2↓ + 2NaCl

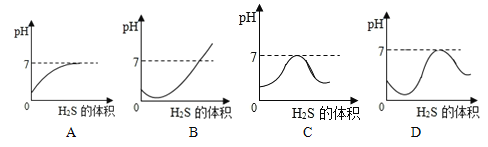
【题目】(题文)小彬同学新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在 学习金属化学性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动。
(查阅资料)
①铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液……
(预测)三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
(实验过程)取大小相同的三种金属片,用砂纸打磨光亮。
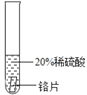
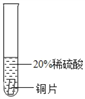
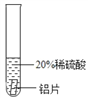
实验一 | 实验二 | 实验三 | |
实 验 方案 |
|
|
|
实 验现象 | ______________ | ____________ | _______ |
结论 | 铬 与 稀 硫 酸 可 以 反应,速度较慢 | 铜不与稀硫酸反应 | _____ |
三种金属在金属活动性顺序表中的相对位置关系是_____ | |||
(回答问题)
(1)将上表中三处划横线的位置填上适当的内容。
(2)用砂纸打磨金属片的目的是_____。
(3)实验一所发生反应的化学方程式是_____。
(4)小东提出用硫酸铝溶液代替上述实验中的稀硫酸,小燕认为不可行,理由是_____。
(5)上述实验用了四种药品,小清认为只要选用三种药品进行实验就可以得出三种金属在 金属活动性顺序表中的相对位置关系,这三种药品可以是_____。
(6)实验发现,相等浓度的盐酸和硫酸,盐酸和铝反应的速率比硫酸快得多,可能的原因是:_____,请设计实验证明你的猜想____________。
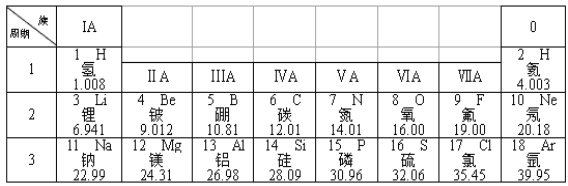
【题目】(题文)(1)请你用最合适的化学式或微粒符号填空:空气中含量最多的气体________;硫酸钠中的阴离子________;改良酸性土壤时常用的一种碱:_________;。
(2)豆浆机由于快捷方便而进入千家万户。请根据图示回答:
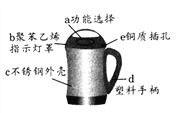
①制作材料中属于金属或合金的是_______(选填一种物质编号),属于有机合成材料的是_________(选填一种物质编号);制作手柄的塑料属于____________塑料(填“热塑性”或“热固性”);
②豆浆已成为众多家庭的早餐饮品,以下是豆浆中一些营养成分的平均质量分数。请根据下表回答:
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素A |
质量分数/% | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
豆浆中含有的微量元素是__________;青少年缺乏______元素易患有佝偻病。在豆浆所含的营养素中能供给人体能量的营养素有______________________。
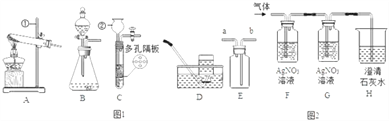
【题目】Ⅰ.请结合下图回答问题。
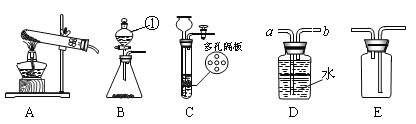
(1)写出图中有标号仪器的名称: ①__________________。
(2)用高锰酸钾制取一瓶干燥的氧气,可选用装置组合为___________(选填序号);实验室制取二氧化碳和氧气可选用发生装置C或B,C装置的优点是__________________,用此装置制取O2的化学方程式是____________________;
(3)实验室常用甲酸(HCOOH)溶液滴加到浓硫酸中制CO气体,可选用的制取装置是______(选填序号)。该反应中浓硫酸既是催化剂又是脱水剂,试写出该反应的化学方程式________________。
Ⅱ.某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
(查阅资料)
(1).CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2),在氢氧化钠较少的情况下会生成蓝绿色碱式氯化铜(Cux(OH)yClz),其不溶于水,能与酸反应。
(2).Cu(OH) 2在60℃开始分解生成两种氧化物,100℃分解完全。碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
(猜想)蓝绿色固体可能是:①Cu(OH)2;②Cux(OH)yClz晶体;③_______。猜想①的理由是:________(用化学方程式表示)。
(验证)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体。则猜想 ________不正确。继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图_____(选填“甲”或“乙”)装置(装置中药品足量)。

(实验数据) ①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g;
③浓硫酸装置中数据如表。
加热前 | 100℃ | 400℃ |
250.00g | 251.80g | 253.60g |
(得出结论)猜想③成立,且碱式氯化铜中X∶Y:Z = _________。
(拓展延伸)
为使实验中生成蓝色固体,少出现蓝绿色固体,应作_______________改进(选填序号)。
a.实验中将氯化铜溶液滴加到氢氧化钠溶液中
b.实验中应提供足量、较浓的氢氧化钠溶液
c.实验应该在80℃的水浴中进行